高纯硅生产流程如下: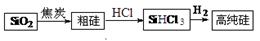
(1)由SiO2制粗硅的化学方程式是 ,该反应不能说明碳的非金属性强于硅,原因是 ,请写出一个能说明碳的非金属性强于硅的化学方程式 。
(2)900℃以上,H2与SiHCl3发生反应:SiHCl3(g)+ H2(g) Si(s) + 3HCl(g) ΔH>0。将一定量的反应物通入固定容积的密闭容器中进行反应。下列说法正确的是 (填字母)。
Si(s) + 3HCl(g) ΔH>0。将一定量的反应物通入固定容积的密闭容器中进行反应。下列说法正确的是 (填字母)。
a.在恒温条件下,若容器内压强不变,则该反应一定达到化学平衡状态
b.增大SiHCl3的用量,可提高SiHCl3的平衡转化率
c.升高温度可加快反应速率,且提高硅的产率
(3)该流程中可以循环使用的物质是 。
在同温同压下,等质量的CO和CO2,其体积之比为,电子数之比为,密度之比为。
将10.6gNa2CO3溶于水配成1L溶液
(1)该溶液中Na2CO3的物质的量浓度为__________,溶液中Na+的物质的量浓度为__________。
(2)向该溶液中加入一定量NaCl固体,使溶液中Na+的物质的量浓度为0.4mol·L-1(假设溶液体积不变)需加入NaCl的质量为__________,Cl-的物质的量浓度为______________________________________________________________。
铅尘污染对人体危害极大,为了减少铅尘污染,各国都在推广使用无铅汽油。所谓无铅汽油是用甲基叔丁基醚代替四乙基铅做抗震剂添加于汽油中,用于提高汽油的辛烷值。甲基叔丁基醚可通过如下方法合成:
(CH3)3CBr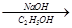 A
A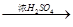 B
B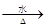 (CH3)3COH
(CH3)3COH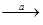 (CH3)3CONa
(CH3)3CONa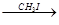 (CH3)3COCH3。
(CH3)3COCH3。
资料支持:
①ROSO3H(R表示烃基) 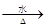 ROH
ROH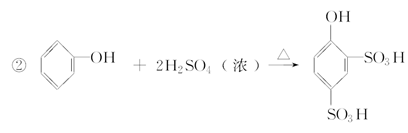
试回答下列问题:
(1)试剂a是________,中间产物A是________。
(2)与产物甲基叔丁基醚互为同分异构体的醇类有________种。
(3)已知由A生成B的反应属于加成反应,则反应的化学方程式为
________________________________________________________________________。
最后一步属于取代反应,则反应的化学方程式为
________________________________________________________________________。
(4)请用流程图表示以苯酚为唯一有机原料合成 (例如由乙醇合成聚乙烯的反应流程图可表示为CH3CH2OH
(例如由乙醇合成聚乙烯的反应流程图可表示为CH3CH2OH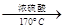 CH2===CH2
CH2===CH2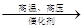 CH2—CH2)。
CH2—CH2)。
A~I九种有机物有如下转化关系: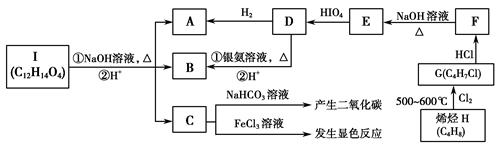
已知:R1CHOHCHOHR2+HIO4―→R1CHO+R2CHO+HIO3+H2O;又知C的核磁共振氢谱图上共有5个峰。
请回答下列问题:
(1)写出下列物质的结构简式:C________;I________。
(2)由H生成G的有机反应类型为_________________________________。
(3)写出下列反应的化学方程式。
D→B过程中的第①步:________________________________________。
G→F:________________________________________________________。
(4)化合物C的同分异构体甚多,写出满足下列条件的所有芳香族同分异构体的结构简式:
________________________________________________________________________。
①属于对位二取代苯;②能发生银镜反应;③在NaOH溶液中可发生水解反应。
由环己烷可制备1,4环己醇二醋酸酯。下面是有关的8步反应(其中所有无机产物都已略去)。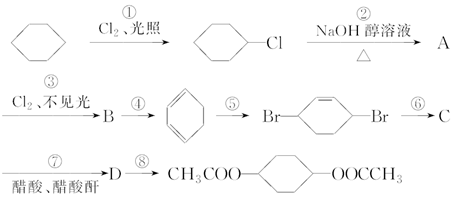
(1)在上述8步反应中,属于取代反应的有________,属于加成反应的有________,反应④属于________反应。
(2)写出下列化合物的结构简式。
B:________,C:________。
(3)写出反应④、⑤、⑥的化学方程式。
④____________________________________________________________,
⑤___________________________________________________________,
⑥__________________________________________________________。
(4)写出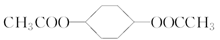 在NaOH溶液中水解的化学方程式:
在NaOH溶液中水解的化学方程式:
__________________________________________________________。