恒容容器中反应:A(g)+3B(g) 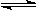 2C(g)+3D(g),达到平衡的标志是
2C(g)+3D(g),达到平衡的标志是
①体系的压强不再改变 ②混合气体的平均相对分子质量不再改变 ③各组分的浓度不再改变 ④混合气体的密度不变 ⑤反应速率vA: vB: vC: vD=1:3:2:3 ⑥单位时间内1 mol A断键反应,同时2 mol C也断键反应
| A.②③⑤⑥ | B.②③④⑤ | C.①④⑤⑥ | D.①②③⑥ |
下列叙述正确的是
| A.1 mol H2O的质量为18g/mol | B.3.01×1023个SO2分子的质量为32g |
| C.CH4的摩尔质量为16g | D.44g CO2含有的O原子数为NA |
只用下列试剂中的一种就能鉴别AgNO3、Na2CO3、K2SO4三种溶液,则该试剂是
| A.KNO3溶液 | B.Na2SO4溶液 | C.NaOH溶液 | D.稀HCl |
现有三组溶液:①汽油和氯化钠溶液 ②70%的乙醇溶液 ③氯化钠和单质碘的水溶液,分离以上各混合液的正确方法依次是
| A.分液、蒸馏、萃取 | B.萃取、蒸馏、分液 |
| C.分液、萃取、蒸馏 | D.蒸馏、萃取、分液 |
下列叙述正确的是
| A.pH相等的盐酸和醋酸溶液中分别加入足量相同的Zn片,反应过程中生成氢气的速率始终相同 |
B.室温下向10mL pH=3的醋酸溶液中加水稀释后,溶液中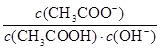 减小 减小 |
| C.醋酸钠溶液中存在反应:CH3COONa+H2O=CH3COOH+NaOH |
| D.在25℃时,将amol/L的氨水与0.01 mol/L的盐酸等体积混合,充分反应后溶液后溶液呈中性则c(NH4+)=c(Cl-) |
常温下,向l00mL 0.01mol/L HA的溶液中逐滴加入0.02mol/L MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中正确的是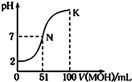
| A.HA为一元强酸,MOH为一元强碱 |
| B.N点水的电离程度小于K点水的电离程度 |
| C.K点所示溶液中c(A-)>c(M+) |
| D.K点对应的溶液中,有c(MOH)+c(M+)=0.01mol/L |