已知下列反应的热化学方程式为
(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol
(2)C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ/mol
(3)H2(g)+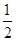 O2(g)=H2O(l) ΔH3=-285.8 kJ/mol
O2(g)=H2O(l) ΔH3=-285.8 kJ/mol
则反应2C(s)+2H2(g)+O2(g)=CH3COOH(l)的ΔH为( )
| A.-488.3 kJ/mol | B.-191 kJ/mol | C.-476.8 kJ/mol | D.-1 549.6 kJ/mol |
实验表明:将氯水滴加到一片蓝色石蕊试纸上,试纸上会出现如图所示的半径慢慢扩大的内外两个圆环,且两环颜色不同,下列有关说法中不正确的是()
| A.此实验表明氯水具有酸性、漂白性 |
| B.内环呈白色外环呈红色或浅红色 |
| C.内外环上颜色的差异表明此变化过程中,中和反应比氧化还原反应快 |
| D.氯水中形成次氯酸的反应中还原产物是HClO |
将3.20g Cu和10.0mol/L的硝酸30.0mL充分反应,还原产物中有NO和NO2。若反应后溶液中有amol  ,则此时溶液中
,则此时溶液中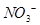 的物质的量为()
的物质的量为()
| A.a/2mol | B.2amol | C.0.100amol | D. |
氯化碘(ICl)的化学性质跟氯气相似,预计它跟水反应的最初生成物是()
| A.HI和HClO | B.HCl和HIO |
| C.HClO3和HIO | D.HClO和HIO |
已知下列反应①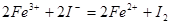 ;②
;②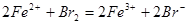 ;
;
③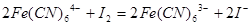 试判断下列物质的氧化性强弱顺序正确的是()
试判断下列物质的氧化性强弱顺序正确的是()
A.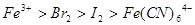 |
B.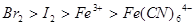 |
C.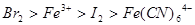 |
D.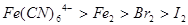 |
下列离子方程式表达不正确的是()
A.小苏打溶液跟烧碱溶液反应: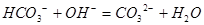 |
B.氢氧化钡溶液跟硫酸反应: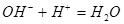 |
C.三氯化铁溶液跟过量氨水反应: |
D.氢氧化铝与氢氧化钠溶液反应: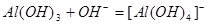 |