分子式C4H8O2的有机物与稀硫酸溶液共热可得有机物A和B。将A氧化最终可得C,且C和B为同系物, 若C可发生银镜反应,则原有机物的结构简式为( )
A.HCOOCH2CH2CH3 B.CH3COOCH2CH3
C.CH3CH2COOCH3 D.HCOOCH(CH3)2
下列各物质中既能发生消去反应又能催化氧化,并且催化氧化的产物能够发生银镜反应的是()
A.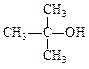 |
B.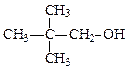 |
C.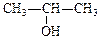 |
D.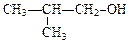 |
据报道,近来发现了一种新的星际分子氰基辛炔,其结构式为HC≡C—C≡C-C≡C-C≡C-C≡N。对该物质判断正确的是()
| A.晶体的硬度与金刚石相当 | B.能使酸性高锰酸钾溶液褪色 |
| C.不能发生加成反应 | D.可由乙炔和含氮化合物加聚制得 |
近期我国冀东渤海湾发现储量达10亿吨的大型油田。下列关于石油的说法正确的是()
| A.石油属于可再生矿物能源 | B.石油主要含有碳、氢两种元素 |
| C.石油的裂化是物理变化 | D.石油分馏的各馏分均是纯净物 |
能在KOH的醇溶液中发生消 去反应的是()
去反应的是()
下列各对物质中,互为同系物的是()
| A.CH3—CH3和CH3—CH=CH2 |
| B.CH3—CH=CH2和 CH3—CH2—CH=CH2 |
| C.CH3—CH2—CH3和CH3—CH=CH2 |
| D.CH3—CH2—CH2—CH3 和 CH3—CH2—OH |