下列说法中,正确的是
| A.强电解质的水溶液一定比弱电解质的水溶液的导电能力强 |
| B.强电解质都是离子化合物,弱电解质都是共价化合物 |
| C.强电解质的水溶液中不存在溶质分子 |
| D.不溶性盐都是弱电解质,可溶性酸和具有极性键的化合物都是强电解质 |
近年来用红外激光技术研究液氢时,发现分子间作用力也可引起微粒间的反应,在液氢中氢分子和质子形成的H3+离子,其构型是等边三角形,属于二电子三中心离子,同时H3+还可进一步形成Hn+,下列判断不正确的是( B )
A.H3+的电子式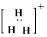 |
| B.H3+可在液氢中形成H4+、H5+、H6+ |
| C.H3+可在液氢中形成H5+、H7+、H9+ |
| D.每个H3+微粒中含有3个质子 |
铅蓄电池的两极分别是Pb、PbO2,电解质溶液为30%硫酸,工作时反应为:
Pb+PbO2+2H2SO4 2PbSO4+2H2O下列结论正确的是(B)
2PbSO4+2H2O下列结论正确的是(B)
| A.PbO2为正极,被氧化 | B.电池电解质溶液的密度不断减小 |
| C.c(H+)逐渐增大 | D.H+向负极移动 |
下列分子中所有的原子都满足最外层为8电子结构的是(B )
| A.BCl3 | B.COCl2 | C.SF6 | D.SiH4 |
关于化学键的叙述中,正确的是(C )
| A.HCl电离产生H+和Cl—,可判断HCl分子中存在离子键 |
| B.Na2O2固体中含有的阴离子与阳离子的个数比为1:1 |
| C.化学键是指使原子或离子相互结合的作用力 |
| D.不同元素组成的多原子分子中的化学键一定全是极性键 |
下列关于原电池说法正确的是(C )
| A.由Al、Mg、稀硫酸组成的原电池,其负极反应式为:Al-3e—=Al3+ |
| B.由Al、Mg、NaOH组成的原电池,其负极反应式为:Al-3e—+3OH—=Al(OH)3↓ |
| C.由Al、Cu、浓硝酸组成的原电池,其负极反应式为:Cu-2e—=Cu2+ |
| D.由Fe、Cu、FeCl3组成的原电池,其正极反应式为:Cu-2e—=Cu2+ |