用于净化汽车尾气的反应:2NO(g)+2CO(g) 2CO2(g)+N2(g),已知该反应的平衡常数极大(570 K时为1×1059),但反应速率极慢。下列说法正确的是
2CO2(g)+N2(g),已知该反应的平衡常数极大(570 K时为1×1059),但反应速率极慢。下列说法正确的是
| A.反应中NO作氧化剂,N2是氧化产物 |
| B.装有尾气净化装置的汽车排出的气体中不再含有NO或CO |
| C.提高尾气净化效率的最佳途径是使用高效催化剂 |
| D.增大压强,上述平衡右移,故可通过增压的方法提高尾气净化效率 |
2011年3月11日日本本州岛附近海域发生强烈地震,强震导致福岛第一核电站发生爆炸引发核危机,其中检测到的放射性元素主要是131I和137Cs,碘在周期表中是53号元素,关于131I和127I的说法正确的是
| A.131I和127I 互为同位素 |
| B.131I和127I都含有53个中子 |
| C.131I和127I分别含有78和74个质子 |
| D.131I和127I含有不同的电子数 |
某链状有机物分子中含有m个 —CH3 ,n个 —CH2— ,a个 ,其余为 —Cl,则—Cl的数目可能
,其余为 —Cl,则—Cl的数目可能
| A.2n+3a-m | B.a+2-m | C.n+m+a | D.a+2n+ 2-m 2-m |
标准状况下,某气态烷烃和烯烃的混合气体2.24L,完全燃烧后生成4.05g水和6.6gCO2,该烃的组成为
| A.CH4、C2H4 | B.C2H6、C2H4 | C.CH4、C3H6 | D.C2H6、C3H6 |
已知卤代烃可以和钠发生反应,例如溴乙烷与钠发生反应为:2CH3CH2Br + 2Na →CH3CH2CH2CH3 +2NaBr;应用这一反应,下列所给化合物中可以与钠合成环丁烷的是
| A.CH3Br | B.CH2BrCH2CH2CH2CH2Br | C.CH2BrCH2Br | D.CH3CH2CH2CH2Br |
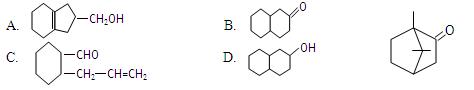
不饱和度(Ω)是衡量有机物分子氢原子饱和程度的尺度,与烷烃及饱和醇相比,分子中每少2个H原子,就有1个Ω,如乙烯、乙醛、苯的不饱和度依次为1、1、4。已知樟脑(C10H16O)的结构如右图,下列4式中与樟脑不属于同分异构体的是