下列关于纯净物、混合物、电解质、非电解质的正确组合为( )
| A.稀硫酸、水煤气、水银、干冰 | B.蒸馏水、蔗糖溶液、氧化铝、二氧化硫 |
| C.胆矾、盐酸、铁、碳酸钙 | D.臭氧、空气、氯化铜、碳酸钠 |
下列化学用语正确的是:
| A.8个中子的碳原子的核素符号:12C | B.H2O的电子式: |
C.Cl-离子结构示意图: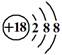 |
D.甲烷的结构式: |
下列有关元素周期表的说法不正确的是:
| A.第一张较完善的元素周期表是俄国化学家门捷列夫绘制的 |
| B.元素周期表中的前20号元素属于短周期元素 |
| C.元素周期表主族元素的最外层电子数等于其主族序数 |
| D.由元素在周期表中的位置可以推导该元素可能具有的化学性质 |
下列有关14C、14N这两种核素的说法正确的是:
A.质量数不相同 B.电子数相同 C.中子数不相同 D.质子数相同
下列说法不正确的是:
| A.绿色化学的核心就是如何对被污染的环境进行无毒无害的治理 |
| B.形成酸雨的主要物质是硫的氧化物和氮的氧化物 |
| C.从海水中可以得到MgCl2,电解熔融MgCl2可制备Mg |
| D.水华、赤潮等水体污染主要是由含氮、磷的生活污水任意排放造成的 |
下列反应的离子方程式正确的是()
| A.钠与水的反应:Na+H2O=Na++OH-+H2↑ |
| B.氯气与水反应:Cl2+H2O=2H++Cl-+ClO- |
| C.氢氧化铝中和胃酸:Al(OH)3+3H+=Al3++3H2O |
| D.用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+ |