某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成,取四份样品分别加稀硫酸反应,其实验数据记录如下表。
| 样品 |
第1份 |
第2份 |
第3份 |
第4份 |
| 取样品质量(g) |
50.0 |
50.0 |
50.0 |
50.0 |
| 取稀硫酸质量(g) |
40.0 |
80.0 |
120.0 |
160.0 |
| 产生气体质量(g) |
0.4 |
0.8 |
1.0 |
1.0 |
试计算:
⑴根据测得的数据分析,第1份样品中 (填物质)完全反应了。
⑵列式计算黄铜屑样品中的锌的质量分数。
⑶请在图中画出在50.0g样品中加稀硫酸的质量与产生气体质量变化关系的示意图。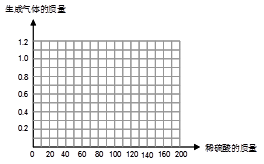
某些厂家为延长食品保质期,常在食品中添加苯甲酸(C6H5COOH)作为防腐剂。回答下列问题:
(1)苯甲酸是由种元素组成;
(2)苯甲酸分子中碳、氢、氧的原子个数比为;
(3)苯甲酸中碳元素与氧元素的质量比为。
某同学欲测定草木灰中碳酸钾的含量,称取69 g试样于烧杯中,加入29.2g稀盐酸恰好完全反应,充分反应后,称得混合物的总质量为93.8 g(忽略二氧化碳的溶解对质量的影响)。请计算:
(1)反应过程中产生的二氧化碳质量为g。
(2)该草木灰试样中碳酸钾的质量分数。
媒体近日报道:市面上部分方便面遭到塑化剂污染,长期接触塑化剂可引起血液系统、生殖系统损害,其中,塑化剂(DMP)分子式为C10H10O4。求:
(1)DMP的相对分子质量为_______;
(2)DMP分子中C、H、O 三种元素的质量比为____________;
(3)DMP分子中氧元素的质量分数为(结果精确到0.01)________。
实验室有一瓶未知浓度的BaCl2溶液,某同学取出 150g该溶液于烧杯中,向其中逐滴加入溶质质量分数为26.5%的Na2CO3溶液。反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如图甲所示。已知:BaCl2+Na2CO3=B
150g该溶液于烧杯中,向其中逐滴加入溶质质量分数为26.5%的Na2CO3溶液。反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如图甲所示。已知:BaCl2+Na2CO3=B aCO3↓+2NaCl请计算:
aCO3↓+2NaCl请计算:
(1)配制26.5%的Na2CO3溶液80g,需要Na2CO3固体g。
(2)BaCl2溶液的溶质质量分数是多少?(写出计算过程,结果保留到0.1%)
苯甲酸(C6H5COOH)是一种酸性比醋酸更强的有机酸,能使紫色石蕊试液变红,常用作食品防腐剂。请回答:
(1)苯甲酸含有种元素。
(2)苯甲酸分子中,C、H、O三种元素的质量比是。
(3)苯甲酸中氧元素的质量分数为(结果保留到0.1%)。