下列有关分散系说法错误的是( )
| A.胶体中分散质的微粒直径在10-9~10-7m之间 |
| B.胶体均一,稳定,静置一段时间后不会产生沉淀 |
| C.蔗糖溶液静置一段时间后,下层会比上层甜 |
| D.可用丁达尔效应来区分FeCl3溶液和Fe(OH)3胶体 |
在同温同压下,某有机物和过量Na反应得到V1 L氢气,另一份等量的该有机物和足量的NaHCO3反应得到V2 L二氧化碳,若V1=V2≠0,则该有机物可能是 ( )
C.HOCH2CH2OH D.CH3COOH
化学反应经常伴随着颜色变化,下列关于颜色的叙述正确的是( )
①鸡蛋白溶液遇浓硝酸——黄色 ②淀粉碘化钾溶液遇碘离子——蓝色 ③FeCl2遇KSCN溶液——血红色 ④热的氧化铜遇乙醇——红色 ⑤新制氯水久置后——无色 ⑥过氧化钠在空气中久置——淡黄色
| A.①④⑤ | B.④⑤⑥ | C.②③④⑥ | D.①②③⑤ |
已知化合物B3N3H6(硼氮苯)与C6H6(苯)的分子结构相似,如图所示:则硼氮苯的二氯取代物B3N3H4Cl2的同分异构体的数目( )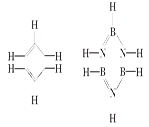
| A.2 | B.3 | C.4 | D.6 |
若乙酸分子中的氧都是18O,乙醇分子中的氧都是16O,二者在浓H2SO4作用下发生酯化反应,一段时间后,分子中含有18O的物质有 ( )
| A.1种 | B.2种 | C.3种 | D.4种 |
在一定温度下的定容密闭容器中,发生反应A(s)+2B(g)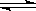 C(g)+D(g),当下列物理量不再变化时,表明反应已达平衡的是 ( )
C(g)+D(g),当下列物理量不再变化时,表明反应已达平衡的是 ( )
①混合气体的压强 ②混合气体的密度③混合气体的平均相对分子质量④气体总物质的量
| A.①② | B.②③ | C.② | D.③ |