已知:
(1)Fe2O3(s) +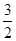 C(s)=
C(s)=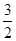 CO2(g)+2Fe(s) ΔH=+234.1 kJ/mol
CO2(g)+2Fe(s) ΔH=+234.1 kJ/mol
(2)C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol
则2Fe(s)+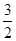 O2(g)=Fe2O3(s) 的ΔH是( )
O2(g)=Fe2O3(s) 的ΔH是( )
| A.-824.4 kJ/mol | B.-627.6 kJ/mol |
| C.-744.7 kJ/mol | D.-169.4 kJ/mol |
把A、B、C、D四块金属浸入稀硫酸中,分别用导线两两相连可以组成原电池。A、B相连时A为负极;C、D相连时,电流由D→C;B、C相连时B极发生氧化反应。这四种金属的活动性顺序是()
A. A﹥B﹥C﹥D B. A﹥C﹥D﹥B C. C﹥A﹥B﹥D D. B﹥D﹥C﹥A
下列含有共价键的离子化合物是()
| A.CO2 | B.CaCl2 | C.NaOH | D.HCl |
燃烧硫铁矿产生SO2 ,为了提高生成SO2的速率,下列措施可行的是()
| A.把块状矿石碾成粉末 | B.降低O2的浓度 |
| C.使用负催化剂 | D.降低温度 |
原电池产生电流的本质原因是()
| A.原电池中溶液能电离出自由移动的离子 |
| B.有导线将两个活动性不同的电极连接 |
| C.正极发生了氧化反应,而负极发生了还原反应 |
| D.两电极上分别进行的氧化、还原反应中会有电子的转移 |
下列电子式书写错误的是( )