强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH-(aq)=H2O(1) △H=-57.3kJ/mol。向1L0.5mol/L的NaOH溶液中加入下列物质:①稀醋酸 ②浓硫酸 ③稀硝酸,恰好完全反应时的热效应△H1、△H2、△H3的关系正确的是
| A.△H1>△H2>△H3 | B.△H1<△H3<△H2 |
| C.△H1<△H2<△H3 | D.△H1>△H3>△H2 |
下图中能验证氯化钠溶液(含酚酞)电解产物的装置是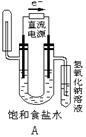


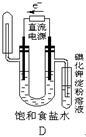
将下图所示实验装置的K闭合,下列判断正确的是
| A.Cu电极上发生还原反应 |
| B.电子沿Zn→a→b→Cu路径流动 |
| C.片刻后甲池中c(SO42-)增大 |
| D.片刻后可观察到滤纸b点变红色 |
某同学组装了如图所示的电化学装置电极I为Al,其他电极均为Cu,则下列说法正确的是
A.电流方向:电极IV→ →电极I →电极I |
| B.电极I发生还原反应 |
| C.电极II逐渐溶解 |
| D.电极III的电极反应:Cu2++2e-==Cu |
如图是甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为2CH3OH +3O2 2CO2+ 4H2O。下列说法不正确的是
2CO2+ 4H2O。下列说法不正确的是
| A.左电极为电池的负极,a处通入的物质是甲醇 |
| B.正极反应式为:O2 + 2H2O + 4e-= 4OH- |
| C.负极反应式为:CH3OH + H2O-6e- = CO2 + 6H+ |
| D.该电池提供1mole-,消耗氧气0.25mol |
蓄电池放电时是起原电池的作用,在充电时起电解池的作用。下式是爱迪生蓄电池分别在充电、放电时的反应: Fe + NiO2 + 2H2O  Fe(OH)2 + Ni(OH)2下列有关爱迪生电池的各种推断中不正确的是
Fe(OH)2 + Ni(OH)2下列有关爱迪生电池的各种推断中不正确的是
| A.放电时铁做负极,NiO2做正极 |
B.充电时阴极上的电极反应为: |
| C.放电时,电解质溶液中的阴离子是向正极方向移动 |
| D.蓄电池的两个电极必须浸入在碱性溶液中 |