有关常温下pH均为11的氨水和Ba(OH)2溶液的说法正确的是
| A.两溶液中,由水电离出的氢氧根离子浓度均为1×10-11mol/L |
| B.分别加水稀释100倍后,两种溶液的pH均变为9 |
| C.氨水中的c(NH+)和Ba(OH)2溶液中的c(Ba2+)相等 |
| D.分别加入等量的pH为1的硫酸,二者的导电能力均减小 |
化学已经渗透到人类生活的各个方面,下列说法正确的是
| A.高纯度的硅单质广泛用于制作光导纤维,光导纤维遇强碱会“断路” |
| B.氮的固定只有在高温、高压、催化剂的条件下才能实现 |
| C.服用铬含量超标的药用胶囊会对人体健康不会造成危害 |
| D.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,既能杀菌消毒又能净水 |
下列实验操作或检验正确的是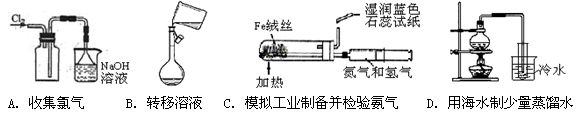
辨析以下的说法:①l6O与l8O的转化可以通过化学反应实现;②灼烧钠的化合物时火焰呈黄色,那是发生了化学反应;③碱性氧化物一定是金属氧化物;④只由一种元素组成的物质一定是纯净物;⑤石墨与金刚石的转化是化学变化。上述说法中正确的是
| A.①④⑤ | B.①③④ | C.③⑤ | D.②③ |
一定量的镁铝合金与足量的氢氧化钠溶液反应产生3.36L氢气。若将等质量的该合金完全溶于稀硝酸,反应中硝酸被还原只产生4.48L的NO(气体的体积均已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为
| A.11.4g | B.16.5g | C.9.7g | D.8.7g |
下列叙述正确的是
A.元素周期表中位于金属与非金属分界线附近的元素属于过渡元素
B.短周期第IVA族与VIIA族元素的原子间构成的分子,均满足原子最外层8电子结构
C.C、N、O、H四种元素形成的化合物一定既有离子键又有共价键
D.第三周期非金属元素含氧酸的酸性从左到右依次增强