小明判断自己乘坐的列车正在向东运动,依据可能是
| A.站台在向东运动 | B.站台在向西运动 |
| C.乘警在向东运动 | D.乘警在向西运动 |
小翔观察小手电筒的电源,由两节干电池串联组成,可知该电筒的工作电压是
| A.0.3V | B.1.5V | C.3V | D.4V |
夏天,我们吃雪糕觉得凉爽,是因为雪糕在口中
| A.液化吸热 | B.熔化放热 | C.凝固吸热 | D.熔化吸热 |
据观察,教室的宽度最接近于
| A.60mm | B.8dm | C.8m | D.60m |
如图所示,电源电压保持不变,只闭合开关S时,电流表的示数为0.2A,若再闭合开关S1,发现电流表的示数为0.5A,此时通过R1的电流为I1,通过R2的电流为I2,则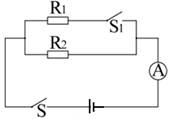
| A.I1:I2=2:5 | B.I1:I2=3:5 |
| C.R1:R2=3:2 | D.R1:R2=2:3 |