已知空气的主要成分是氮气和氧气。某课外活动小组设计了测定空气中氧气含量的实验,实验装置如下图所示。
(1)红磷在集气瓶中发生反应的文字表达式为: [来该实验中红磷需稍过量。目的是 。
(2)待燃烧停止,白烟消失并冷却后,打开止水夹,观察到烧杯中的水进入集气瓶,瓶内水面最终接近刻度1处。由此可知,氧气约占空气总体积的五分之一,由本实验还可推知氮气的哪一些性质?试写出其中的一种:
(3)若将红磷换成碳粉,该实验不能成功的理由是: 。
苯胺是橡胶助剂、医药磺胺药及生产农药的重要原料,苯胺的化学式为C6H5NH2.苯胺对环境有危害,对水体可造成污染,会引起人体高铁血红蛋白血症、溶血性贫血和肝、肾损害.请根据苯胺的化学式,回答下列问题:
(1)苯胺是由种元素组成。
(2)苯胺中C、H、N元素的质量比。
(3)苯胺中碳元素的质量分数是(结果保留到0.1%)。
实验室常用如图所示A、B装置制取气体,回答相关问题:
(1)图中①的仪器名称是。
(2)小敏用A装置制取较纯净、干燥的氢气,反应的化学方程式为;在瓶②内要盛装;请在方框内将收集装置中的导管补画完整。
(3)连接装置应按照、从左到右的顺序安装,并检查装置的气密性。
(4)装置B用于实验室制取氧气.反应完毕后,可以回收二氧化锰继续使用的原因是。
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3).你认为利用装置B是否可行?(填“是”或“否”),理由是。
重铬酸钾(K2Cr2O7)是一种橙红色固体,它在实验室中和工业上都有很广泛的应用。
(1)重铬酸钾属于(填“氧化物”、“酸”、“碱”或“盐”);
(2)重铬酸钾中铬元素的化合价为价;
(3)铬元素属于人体中的(填“微量元素”或“有害元素”);
(4)在加热条件下,重铬酸钾分解反应的化学方程式为:4K2Cr2O7 4K2CrO4+2Cr2O3+3X↑,则X的化学式为。
4K2CrO4+2Cr2O3+3X↑,则X的化学式为。
(5)重铬酸钾的硫酸溶液用于检查是否酒后开车,是因为酒精与该溶液反应生成绿色的硫酸铬(铬元素显+3价),该检查仪器中的废液可用氢氧化钠溶液处理.写出硫酸铬与氢氧化钠溶液发生复分解反应的化学方程式。
根据图A、B、C三种固体的溶解度曲线回答: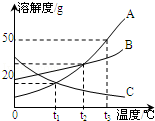
(1)在某一温度时,A、B两饱和溶液的溶质质量分数相等,此时为℃。
(2)在t1℃~t2℃范围内,A、B、C三种物质的溶解度由大到小的顺序为。
(3)要使C的饱和溶液变为不饱和溶液,可采用的一种方法是。
(4)要从含有少量A的B溶液中得到较多的B晶体,通常采用的方法是。
(5)t3℃时,将30gA加入到装有50g水的烧杯中,充分搅拌,所得溶液的溶质质量分数为(结果精确至0.1%)。
(6)在室温时将A物质加入到盛水的烧杯中,充分搅拌后发现仍有少量A未溶解,但放置一段时间后,发现A完全溶解了,可能的原因是。
下表列出了人体中含量较高的几种元素的原子结构示意图,回答下列问题.
| H |
C |
Na |
Cl |
O |
K |
Ca |
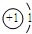 |
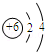 |
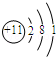 |
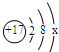 |
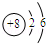 |
 |
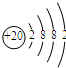 |
(1)x=。
(2)人体中含量最多的物质化学式为;19号元素形成离子的化学符号为。
(3)幼儿及青少年缺钙会患病和发育不良。
(4)检验由钠、氯元素组成的化合物通常选用的试剂是(填化学式)和稀硝酸。
(5)碳元素组成的物质众多,如图表示碳元素组成的两种单质的转化过程:C(石墨)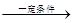 C(金刚石),
C(金刚石),
由此可得出对化学变化的微观解释。