下图所示为实验室中常见的气体制备和收集装置。
请回答下列问题:
(1)实验室用高锰酸钾制取氧气,应选用发生装置 (填字母序号),反应的化学方程式为 。若用装置D收集氧气,验满的方法是 。
(2)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,你认为选用C的优点是 。
(3)欲使用装置E用排空气法收集氢气,则气体应从 (填“a”或“b”)端通入;欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从 (填“a”或“b”)端通入。
(4)已知一氧化氮气体难溶于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时应选用图中装置 (填字母序号)。
(4分)我省南丰蜜桔名扬四海,号称“世界蜜桔之王”。它富含铁、磷、钙等元素,同时含葡萄糖、柠檬酸、维生素C、氨基酸、水等。请用恰当的化学用语表示下列带点部分:
(1)磷元素;
(2)柠檬酸中含有氢离子;
(3)水中氧元素的化合价为-2价;
(4)6个碳原子、12个氢原子、6个氧原子构成一个葡萄糖分子,葡萄糖的化学式为。
根据下列装置图回答问题: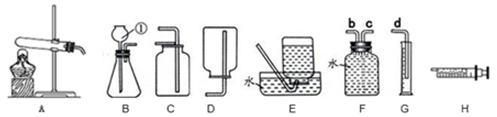
(1)标号为①的仪器名称是。
(2)注射器H可用于检查装置B的气密性,步骤如下:
①向锥形瓶中加入少量水至处。
②将注射器H连接到装置B的导管口处。
③缓慢向外拉动注射器H的活塞,观察到,表示装置B的气密性良好。
(3)实验室用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,其发生装置可选择(填字母序号),甲烷气体可选择E装置进行收集,收集满后集气瓶的放置方式如下图,由此可推断甲烷一定具备的物理性质是、。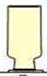
(4)实验室用一定质量的高锰酸钾制取氧气,通过排水量测定所收集到的氧气体积(装置选用A、F、G)。
①写出该反应的化学方程式。
②若各装置的连接顺序是:a→b→c→d,F装置内导管(“b”或“c”)该怎样延伸?请画出。
③根据高锰酸钾的质量算出的氧气体积为理论值。如果实际测得(水的体积测量准确),你认为原因是。
(5)若改用氯酸钾和二氧化锰来制取氧气,则二氧化锰在反应前后固体混合物中的质量分数将(填“变大”、“变小”或“不变”)。实验室若用装置B制取O2时,如用注射器H代替长颈漏斗,优点是。
在实验室中,下列做法正确的是。
| A.配制硫酸溶液时,可先在量筒内加入一定体积的水,再在搅拌条件下慢慢加入浓硫酸。 |
| B.可将废酸液和废碱液相互混合,混合后测其pH约为7,再用水稀释后即可排放 |
| C.连接仪器时,橡胶塞用水润湿后慢慢旋进试管口 |
| D.切忌向燃着的酒精灯内添加酒精,可用燃着的酒精灯去点燃另一盏酒精灯 |
E.实验室制取气体时,应先检查装置的气密性后再装药品
F.各放一张质量相同的纸于天平的左右托盘上,将氢氧化钠固体放在左盘的纸上称量
G.胶头滴管用完后不洗涤就直接插入原滴瓶
H.用托盘天平称量时,砝码应先加质量大的,再加质量小的
某化学兴趣小组进行了识别化肥的探究活动.他们对氯化铵、碳酸氢铵、硫酸钾、
磷矿粉四种化肥的实验探究步骤如下:
(1)步骤一:取上述四种化肥各少量分别放入试管,观察,从外观上即可与其他化肥区分出来的是。
(2)步骤二:在装有另外三种化肥的试管中,分别加入少量稀盐酸,有气体产生的是。
(3)步骤三:再分别取少量未区分出的另外两种化肥于研钵中,各加入少量熟石灰粉末,混合、研磨,有刺激性气味气体放出的是,由此可知,在使用该类化肥时,要避免与(填“酸”或“碱”)性物质混合施用,以防降低肥效。有同学提出,氯化铵、硫酸钾也可用下列某种物质进行区分,你认为可行的是。
| A.硝酸钡溶液 | B.氯化钠溶液 | C.酚酞溶液 | D.稀盐酸. |
物质王国举行一场趣味篮球赛.某队由铁、二氧化碳、稀硫酸、氢氧化钙、氯化铜五名“队员”组成,比赛中,由氯化铜“队员”发球,“队员”间传接球,最后由D位置“队员”投篮进球完成有效进攻.传接球“队员”间物质必须能相互反应,场上“队员”位置及传球路线如图.
(1)已知D位置上投篮的“队员”是个灭火“能手”,则D位置“队员”代表的物质是___;
(2)C 位置“队员”所代表的物质的一种用途是____;
(3)写出连线③代表的物质间发生反应的化学方程式____,
(4)连线①代表的物质间发生反应的化学反应的基本类型是___ _反应;
(5)为实现“快速进攻”,氯化铜除传球给A位置“队员”外,还能直接传球给___ _ “队员”(填物质名称)