下列说法正确的是( )
| A.等物质的量的CH4与Cl2恰好反应时只生成CH3Cl与HCl |
| B.羟基(一OH)和氢氧根(OH一)的电子数不同 |
| C.苯和乙烯都能与溴水发生反应而使溴水褪色 |
D. 与 与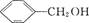 互为同系物 互为同系物 |
No为阿伏加德罗常数的值。下列叙述正确的是
| A.1 mol氢氧根离子与1 mol羟基所含电子数均为l0No |
| B.2.8gN2和CO的混合物中,所含分子总数为0.2No |
| C.标准状况下,11.2 L甲醛气体所含σ键数目为1.No |
| D.2.24 L C02与足量的Na202反应,转移的电子总数必为0.1No |
七种短周期元素在元素周期表中的相对位置如表所示。其中B的最高价氧化物的水化物能与B的气态氢化物反应生成离子化合物,下列说法正确的是
A.氧化物对应的水化物的酸性:G一定强于F
B.简单离子的半径:F>G>C>D
C.1 mol EC2中含2 mol E-C键
D.A、G分别与氢元素形成的化合物中,化学键均为极性共价键
已知,H2和I2反应的历程为:①I2+M 2I·+M慢 ②H2+2I·→2HI快,式中M是指反应器壁或其他惰性分子,不参与反应,只具有传递能量的作用。下列关于该反应的说法正确的是
2I·+M慢 ②H2+2I·→2HI快,式中M是指反应器壁或其他惰性分子,不参与反应,只具有传递能量的作用。下列关于该反应的说法正确的是
| A.反应速率与I·的浓度有关 |
| B.M是该反应的催化剂 |
| C.反应①与②的活化能相等 |
| D.v(H2)=v(I2)=v(HI) |
中国科学家屠呦呦因创制了具有国际影响的新型抗疟药——青蒿素和双氢青蒿素,获得2015年诺贝尔生理学或医学奖。青蒿素的结构如图所示,下列关于青蒿素的说法错误的是
| A.分子中含有3种官能团 |
| B.易溶于苯,难溶于水 |
| C.可与NaOH溶液发生水解反应 |
| D.其同分异构体不可能有芳香族化合物 |
食品抗氧化剂是能阻止或延缓食品氧化变质、提高食品稳定性和延长贮存期的食品添加剂。下列物质不属于食品抗氧化剂的是
| A.糕点中的配料维生素C |
| B.方便面里的味精(谷氨酸钠) |
| C.葡萄酒中的少量二氧化硫 |
| D.火腿肠中的少量亚硝酸钠 |