设阿伏加德罗常数的值为NA,下列说法中正确的是( )
A.1mol苯乙烯(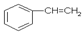 )中含有的碳碳双键数为4NA )中含有的碳碳双键数为4NA |
| B.0.1molCnH2n+2中含有的碳碳单键数为0.1n NA |
| C.2.8 g乙烯和聚乙烯的混合物中所含碳原子数为0.2NA |
| D.标准状况下,2.24LCHCl3含有的分子数为0.1NA |
下列设备工作时,将化学能转化为热能的是
四种短周期元素在周期表中的位置如图,其中只有M为金属元素。下列说法正确的是
| A.原子半径Z>Y |
| B.X的最简单气态氢化物的热稳定性比Z的强 |
| C.M与Z形成的化合物中只存在离子键 |
| D.M的最高价氧化物对应水化物不能与NaOH溶液反应 |
下列说法中正确的是
| A.氯化氢溶于水能电离出H+、Cl-,所以氯化氢是离子化合物 |
| B.碘晶体受热转变成碘蒸气,吸收的热量用于克服碘原子间的作用力 |
| C.氧气和臭氧是同分异构体 |
| D.有机化合物CH3-CH2-NO2和H2N-CH2-COOH是同分异构体 |
下列粒子中与NH4+具有相同质子数和电子数的是
| A.Na+ | B.H2O | C.OH- | D.Al3+ |
可以证明某化合物一定含有离子键的性质是
| A.具有较高的熔点 | B.熔融状态能导电 |
| C.可溶于水 | D.溶于水能导电 |