下列两种物质的溶液混合后不能发生离子反应的是( )
| A.HNO3和Na2CO3 | B.NaCl和AgNO3 |
| C.K2SO4和BaCl2 | D.HNO3和BaCl2 |
向50mL 18 mol/L H2SO4溶液中加入足量的锌粒(可加热)充分反应后生成的气体的物质的量为
| A.小于0.45 mol | B.等于0.45 mol |
| C.在0.45 mol和0.90 mol之间 | D.等于0.90 mol |
将一定量A、B装入容积为1 L的恒温密闭容器中,发生反应:2A (s)+bB (g) cC (g),1 min时达到平衡,C的浓度为x mol·L-1。若保持温度不变,将密闭容器的容积压缩为原来的一半,重新达到平衡后,C的浓度为2.5x mol·L-1。下列说法正确的是
cC (g),1 min时达到平衡,C的浓度为x mol·L-1。若保持温度不变,将密闭容器的容积压缩为原来的一半,重新达到平衡后,C的浓度为2.5x mol·L-1。下列说法正确的是
A.化学计量数的关系:b<c
B.容器的容积减小后,该反应的逆反应速率减小
C.若保持温度和容器的容积不变,充入氦气(不参与反应),平衡不发生移动
D.原容器中用B的浓度变化表示该反应在1 min内的速率为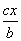 mol·L-1·min-1
mol·L-1·min-1
常温下,0.1 mol·L-1某一元酸(HA)溶液中c(OH-)/c(H+)=1×10-8,下列叙述正确的是
A.该溶液中水电离出的c(H+)=1×10-10 mol·L-1
B.该溶液中c(H+)+c(A-)+c(HA)=0.1 mol·L-1[
C.该溶液与0.05 mol·L-1 NaOH溶液等体积混合后:c(A-)>c(Na+)>c(OH-)>c(H+)
D.向该溶液中加入一定量NaA晶体或加水稀释,溶液中c(OH-)均增大
某无色溶液,由Na+、Ba2+、Al3+、AlO2-、Fe3+、CO32-、SO42-中的若干种组成。取适量该溶液进行如下实验:①加入过量盐酸,有气体生成;②在①所得的溶液中再加入过量碳酸氢铵溶液,有气体生成,同时析出白色沉淀甲;③在②所得溶液中加入过量Ba(OH)2溶液,也有气体生成,并有白色沉淀乙析出。原溶液中一定存在的离子是
| A.Al3+、Fe3+、SO42- | B.Na+、AlO2-、CO32- |
| C.Na+、AlO2-、SO42-、CO32- | D.Na+、Ba2+、AlO2- |
下列有关化学反应现象和化学原理运用的叙述一定有误的是
| A.漂粉精的有效成分是Ca(ClO)2,Ca(ClO)2难分解,但漂粉精仍需密封保存 |
| B.不锈钢是利用了牺牲阳极的阴极保护法来达到防止腐蚀的目的 |
| C.无机非金属材料光导纤维能够被氢氟酸腐蚀 |
| D.石灰石高温煅烧能分解,与此反应是熵增反应有关 |