某微粒用符号ZAMn+表示,下列关于该微粒的叙述正确的是
| A.所含质子数为(A-n) | B.所含中子数为(A-Z) |
| C.所含电子数为(Z+n) | D.中子数-电子数=A-2Z-n |
已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-Q kJ·mol-1 (Q>0),下列说法正确的是
2SO3(g) ΔH=-Q kJ·mol-1 (Q>0),下列说法正确的是
| A.相同条件下,2 mol SO2(g)和1 mol O2(g)所具有的能量小于2 mol SO3(g)所具有的能量 |
| B.将2 mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后,放出热量为Q kJ |
| C.增大压强或升高温度,该平衡都向逆反应方向移动 |
| D.将一定量SO2(g)和O2(g)置于密闭容器中充分反应放热Q kJ此时有2 mol SO2(g)被氧化 |
下列实验事实所得出的结论中,错误的是
| A.向A gCl沉淀中滴入稀KI溶液白色沉淀变黄,说明AgI比AgCl更难溶 |
| B.加入盐酸,产生能使澄清石灰水变浑浊的无色气体,则试样中一定有CO32- |
| C.先加入盐酸无 沉淀,再加入Ba Cl2溶液产生白色沉淀,则试样中一定有SO42- |
| D.盐溶液中加入NaOH微热,产生使湿润的红色石蕊试纸变蓝的气体,则一定是铵盐 |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.无色溶液中:K+、H+、Fe2+、NO3- |
| B.c(H+)<c(OH-)的溶液中:Na+、K+、SO42-、ClO- |
| C.含0.1mol·L-1 HCO3-的溶液中:Al3+、Ca2+、NO3-、SO42- |
| D.含0.1 mol·L-1 SCN-的溶液中:Fe3+、NH4+、NO3-、Cu2+ |
在10L密闭容器中,A、B、C三种气态物质构成可逆反应体系,其关系如图所示。下列说法错误的是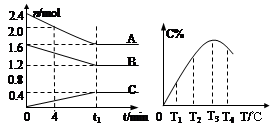
A.0~4分钟时,A的平均反应速率为0.01mol·L-1·min-1
B.由T1向T2变化时,V正>V逆
C. 此反应的正反 应为吸热反应
D.其它条件不变,加压,达新平衡时,C的体积分数增大
用铁丝、铜丝和CuSO4溶液可以构成原电池或电解池,如图所示则下列说法正确的是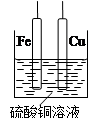
| A.构成原电池时Cu极反应为:Cu—2e-=Cu2+ |
| B.构成电解池时Cu极质量可能减少也可能增加 |
| C.构成电解池时Fe极质量一定减少 |
| D.构成的原电池或电解池工作后就可能产生大量气体 |