、某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g)  Z(g)+W(s);ΔH>0 下列叙述正确的是
Z(g)+W(s);ΔH>0 下列叙述正确的是
| A.加入少量W,逆反应速率增大 |
| B.当容器中气体压强不变时,反应达到平衡状态 |
| C.升高温度,平衡逆向移动 |
| D.平衡后加入X,上述反应的ΔH增大 |
下图中X、Y分别是直流电源的两极,通电后发现a电极质量增加,b电极处有无色无味气体放出。符合这一情况的是表中的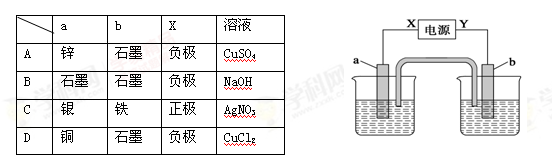
完全燃烧一定质量的无水乙醇,放出的热量为Q,为完全吸收生成的CO2,并使之生成正盐Na2CO3,消耗掉0.8mol/L NaOH溶液500mL,则燃烧1mol酒精放出的热量是
| A.0.2Q | B.0.1Q | C.5Q | D.10Q |
如图所示,烧杯中盛有海水,铁在其中被腐蚀由快到慢的顺序为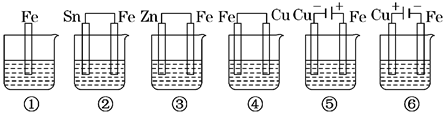
| A.②①③④⑤⑥ | B.⑤④③①②⑥ |
| C.⑤④②①③⑥ | D.⑤③②④①⑥ |
25 ℃时,向纯水中加入NaOH,使溶液的pH为11,则由NaOH电离出的OH-离子浓度与水电离的OH-离子浓度之比为
| A.1010∶1 | B.5×109∶1 | C.108∶1 | D.1∶1 |
有A,B,C,D四种金属。将A与B用导线连接起来浸入电解质溶液中,B不易腐蚀,将A,D分别投入等浓度的盐酸中,D比A反应剧烈,将铜浸入B的盐溶液中,无明显变化,若将铜浸入C的盐溶液中,有金属C析出。据此判断这四种金属的活动性由强到弱的顺序是
| A.D>C>A>B | B.D>A>B>C | C.D>B>A>C | D.B>A>D>C |