一定条件下,体积为10L的密闭容器中,1molX和1molY进行反应:2X(g)+Y(g)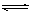 Z(g),经60s达到平衡,生成0.3molZ。下列说法正确的是
Z(g),经60s达到平衡,生成0.3molZ。下列说法正确的是
| A.以X浓度变化表示的反应速率为0.001mol/(L·s) |
B.将容器体积变为20L,Z的平衡浓度变为原来的 |
| C.若增大压强,则物质Y的转化率减小 |
| D.若升高温度,X的体积分数增大,则该反应的△H>0 |
在化学学习中使用数轴的表示方法可收到直观、形象的效果,下列表达中正确的是
A.分散质微粒的大小与分散系种类的关系: |
B.常温下溶液的pH其酸碱性的关系: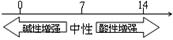 |
C.硫的化合物中化合价与其氧化性、还原性的关系: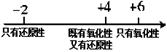 |
D.Fe在Cl2中燃烧的产物与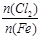 的关系: 的关系: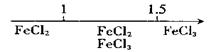 |
实验是化学研究的基础,关于下列各装置图的叙述中,正确的是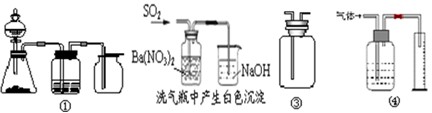
| A.装置①是一套实验室制气装置,用于发生、干燥和收集气体,如铜屑与稀硝酸 |
| B.装置②中,白色沉淀为BaSO3 |
| C.装置③可用于收集H2、NH3、Cl2、HCl、NO2等 |
| D.装置④能用于测量气体体积的装置 |
下列说法可以实现的是
①酸性氧化物在一定条件下均能与碱发生反应
②弱酸与盐溶液反应可以生成强酸
③发生复分解反应,但产物既没有水生成,也没有沉淀和气体生成
④两种酸溶液充分反应后,所得溶液呈中性
⑤有单质参加的反应,但该反应不是氧化还原反应
⑥两种氧化物发生反应有气体生成
| A.①②③④⑤⑥ | B.只有①②④⑤ | C.只有③④⑤⑥ | D.只有②④⑤ |
化学与生产、生活、社会密切相关,下列说法正确的是
| A.氯气可用于漂白,是因为氯气有强氧化性 |
| B.工业用石灰石、纯碱和石英在高温下制得玻璃的原理与硅酸和碳酸的酸性强弱有关 |
| C.神七宇航员所穿航天服是由我国自行研制的新型“连续纤维增韧”航空材料做成,其主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料。 |
| D.硫酸工业中,从吸收塔上部导出的气体再次通入接触室进行二次氧化,进一步吸收后,二氧化硫的含量很少,可直接排放到空气中 |
下列叙述中完全正确的一组是
①常温常压下,1 mol甲基(—CH3)所含的电子数为10NA
②由Cu、Zn和稀硫酸组成的原电池工作时,若Cu极生成0.2gH2,则电路通过电子0.2NA
③5.6克铁粉与硝酸反应失去的电子一定是0.3NA
④常温常压下,16 g O2和O3所含的原子数为NA
⑤1 mol C10H22分子中共价键总数为31 NA
⑥1 mol Cl2发生反应时,转移的电子数一定是2 NA
⑦标准状况下,22.4 L水中含分子数为NA
| A.②③④ | B.②③⑥⑦ | C.①②④⑤ | D.②③④⑤ |