(1)已知碳-12 原子的质量是 1.993×10-26 kg,,A原子的质量是5.146×10-26 kg,若A原子核内中子数比质子数多1,求:(写出计算过程)
①A原子的相对原子质量
②A原子的核外电子数
(2)某市的“二期课改”中,初中化学引入“物质的量”的教学内容。物质的量是一种新的物理量,其单位是摩尔(mol),1摩尔物质大约含有6.02×1023个该物质的微粒。如1mol氢气含有6.02×1023个 H2分子,含有2×6.02×1023个氢原子。据此回答 :(①②两问用计算式表示)
①1mol水(化学符号是H2O)中含有 个氢原子,含有 个氧原子。
②1mol氧分子(化学符号是O2)分子中含有 个电子。
化学实验室加热用的酒精灯里的燃料是乙醇,化学式为CH3CH2OH,相对分子质量为46,试计算
(1)一个乙醇分子里含有 原子.
(2)该物质有 种元素组成,它属于 (填“有机物”或“无机物”).
(3)乙醇中碳元素的质量分数为 .
2012年11月18日,贵州省六盘水某煤矿发生瓦斯爆炸事故,其中17人下落不明.瓦斯(化学式为X)燃烧时发生如下反应:
X+2O2═CO2+2H20,X的化学式为 ,为了防止瓦斯爆炸,煤矿的矿井里必须采取 等安全措施.
在初中化学中,我们学习了有关溶质的知识,如图是硝酸钾的溶解度曲线: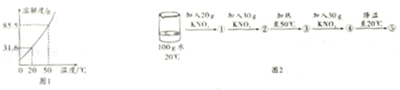
(1)从图1中可得到的信息是(任写一条) .
(2)某同学进行了如图2的实验.实验过程中,属于不饱和溶液的是 (填序号)
(3)下列操作能使⑤中溶质质量分数改变的是
| A.加入20g KNO3 | B.加入50g水 |
| C.升高温度 | D.加入100g30℃的甲的饱和溶液,在恢复到20℃ |
钢铁的产量是体现一个国家生产力的重要指标,但钢铁的锈蚀与保护仍将是我们面临的重大问题.
(1)把一块表面锈蚀的铁片放入过量的盐酸中,观察到的现象是 ,该反应的化学方程式为 .
(2)将生锈的铁钉浸泡在稀盐酸中,过一段时间后,观察到铁钉表面冒气泡,这是因为铁锈除完后与里层的铁反应.由此可知,用盐酸浸泡法除去钢铁表面的铁锈时应注意 .
我区威宁盛产马铃薯,马铃薯有相当的营养价值.马铃薯含有丰富的糖类、铁、胡萝卜素、维生素等.
(1)马铃薯中含有的营养成分能为人提供能量的是 .
(2)人体中缺少铁元素易导致 .
(3)胡萝卜素(化学式为C40H56)中C元素的质量分数是 .