2010年3月30日,我国研究人员发表报告认为,全球将有1.4亿人因为用水而受到砷中毒之害、导致更多的人患癌症。海带含砷超标,经水浸泡24小时后,其含砷量才能达到食用安全标准。下列对砷(As)的有关判断正确的是 ( )
| A.砷原子序数为33,第4周期第5A族 | B.砷酸化学式为H2AsO4 |
| C.砷化氢的稳定性比溴化氢的强 | D.砷酸的酸性比硫酸的弱 |
在下列条件下,各离子组一定能大量共存的是
A.强碱性溶液中:K+、Al3+、Cl-、SO42- |
B.室温下,pH=0的溶液中: Na+、Fe3+、NO3-、SO42- |
C.含有1 mol·L-1 Fe3+的溶液中:K+、Mg2+、I-、NO3- |
D.由水电离的c(H+)=1×10-14的溶液中:K+、Ca2+、Cl-、HCO3- |
下列叙述正确的是
| A.Na在氧气中燃烧主要生成Na2O | B.将SO2通入BaCl2溶液可生成BaSO3沉淀 |
| C.将Fe粉和S粉混合后加热可生成FeS | |
| D.将Na投入到CuSO4溶液中能使Cu2+还原成Cu析出 |
下列各项操作中,发生“先产生沉淀,然后沉淀又溶解”现象的是 ① 向Ca(ClO)2溶液中通入过量CO2② 向AlCl3溶液中逐滴加入过量氨水
① 向Ca(ClO)2溶液中通入过量CO2② 向AlCl3溶液中逐滴加入过量氨水 ③ 向AgNO3溶液中逐滴加入过量氨水④ 向Na2SiO3溶液中逐滴加入过量的盐酸
③ 向AgNO3溶液中逐滴加入过量氨水④ 向Na2SiO3溶液中逐滴加入过量的盐酸 
| A.只有②③ | B.只有①③ | C.只有①②③ | D.①②③④ |
下列反应: ①金属钠与水反应 ②过氧化钠和水反应 ③二氧化氮和水反应 ④氯气和水反应 ⑤三氧化硫和水反应,其中属于氧化还原反应,但水既不是氧化剂,又不是还原剂的是
| A.全部 | B.②③④⑤ | C.只有②③④ | D.只有③④ |
用下图表示的一些物质或概念间的从属关系中不正确的是 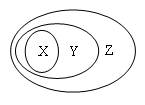
| X |
Y |
Z |
|
| A |
苯的同系物 |
芳香烃 |
芳香族化合物 |
| B |
胶体 |
分散系 |
混合物 |
| C |
电解质 |
离子化合物 |
化合物 |
| D |
碱性氧化物 |
金属氧化物 |
氧化物 |