阿伏加德罗常数为NA,下列叙述中不正确的是 ( )
①12g石墨烯(单层石墨)中含有六元环的个数为0.5 NA
②0.5 mol·L—1 Mg(NO3)2溶液中含有为2NA
③7.8 g Na2S和Na2O2的固体混合物中含有的阴离子数大于0.1NA
④2mol SO2和1 mol O2混合在V2O5存在的条件下于密闭容器中加热反应后,容器内物质分子数大于2NA
⑤足量Fe与0.1 mol氯气反应时失去的电子数为0.3 NA
⑥含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1 NA
⑦agC2H4和C3H6的混合物所含共用电子对数目为3aNA/14
| A.①④⑦ | B.①③④⑤⑥ | C.②③⑤⑥ | D.③④⑤⑥ |
“NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl”是著名的“侯氏制碱法”的重要反应。下面是4位同学对该反应涉及的有关知识发表的部分见解。其中不正确的是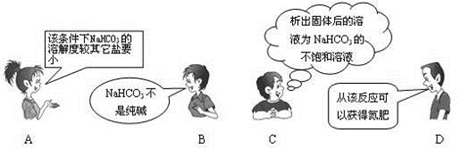
下列各组离子在溶液中能大量共存的是
| A.H+ , SiO32-, Na+ , Cl- |
| B.Fe3+ , Mg2+ , SCN-, SO42- |
| C.K+ , Ca2+ , CO32-, Cl- |
| D.Al3+, Fe2+ , NO3-, SO42- |
下列反应中,反应后固体物质增重的是
| A.氢气通过灼热的CuO粉末 |
| B.二氧化碳通过Na2O2粉末 |
| C.将锌粒投入Cu(NO3)2溶液 |
| D.碳酸氢钠固体加热至没有气体放出 |
下列物质在生产、生活和科技等方面的叙述不正确的是
| A.生铁、普通钢和不锈钢中的碳含量依次增加 |
| B.硅酸钠的水溶液俗称水玻璃,可用作木材防腐剂 |
| C.节日燃放的烟花是某些金属元素发生焰色反应所呈现出来的色彩 |
| D.明矾在自然水中生成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
下列实验操作合理的是
| A.用稀硫酸清洗做焰色反应的铂丝 |
| B.用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 |
| C.用100mL容量瓶配制50mL 0.1 mol·L-1的盐酸 |
| D.测NaOH熔点时可以将NaOH放入石英坩埚中高温熔化 |