在一定温度下可逆反应N2+3H2 2NH3已达到平衡,下列有关说法正确的 ( )
2NH3已达到平衡,下列有关说法正确的 ( )
①1个N≡N键断裂的同时,有3个H—H键形成
②反应混合物中各组分的体积分数保持不变
③恒温恒容时,容器内的压强不再改变
④1个N≡N键断裂的同时,有3个N—H 键形成
⑤NH3生成的速率与NH3分解的速率相等
⑥单位时间生成n molN2,同时生成2n molNH3
⑦气体的平均相对分子质量不再改变
⑧N2 H2 NH3的分子数一定为1∶3∶2
⑨恒温恒容时,气体的总物质的量不再改变
⑩恒温恒压时,容器内的密度不再改变
| A.①②③④⑤⑥⑦⑨ | B.①②③⑤⑥⑩ |
| C.③④⑤⑥⑦⑧ | D.①②③⑤⑥⑦⑨⑩ |
向物质的量浓度均为1 mol·L-1的AlCl3和盐酸的混合溶液中逐滴滴入NaOH溶液,如图中[n表示Al(OH)3的物质的量、V表示NaOH溶液的体积]能正确表示这个反应过程的是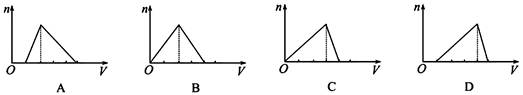
利用下列各组物质制备和收集少量相应气体,能采用如图实验装置的是
| A.浓氨水与固体CaO | B.FeS与稀硫酸 |
| C.稀硝酸与铜片 | D.电石与水 |
下列各种物质在一定条件下反应,所得产物种类与反应物的用量无关的是
①AlCl3(aq)+NH3(g)②Na2SiO3+HCl③C+O2
④Fe+HNO3⑤Ca(HCO3)2+Ca(OH)2⑥C+SiO2
| A.①②⑤ | B.②③ | C.①⑤⑥ | D.④⑤ |
下列实验设计及其对应的离子方程式均正确的是
| A.用FeCl3溶液腐蚀铜线路板:Cu+Fe3+=Cu2++Fe2+ |
| B.Na2O2与H2O反应制备O2:Na2O2+H2O=2Na++2OH-+O2↑ |
| C.将氯气溶于NaOH溶液制备漂白粉:Cl2+2OH-=H2O+Cl-+ClO- |
| D.用稀硫酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
下列离子或分子在溶液中能大量共存,通入CO2后仍能大量共存的一组是
| A.K+、Ca2+、F-、NO3- | B.K+、Ba2+、Br-、NO3- |
| C.Na+、K+、CO32-、HCO3- | D.Na+、Ag+、NH3·H2O、NO3- |