将等物质的量浓度的CuSO4溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图,则下列说法正确的是( )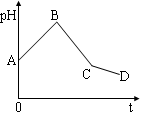
| A.阳极产物一定是Cl2,阴极产物一定是Cu |
| B.BC段表示在阴极上是H+放电产生了H2 |
| C.整个过程中阳极先产生Cl2,后产生O2 |
| D.CD段表示阳极上OH一放电破坏了水的电离平衡,产生了H+ |
设NA是阿伏加德罗常数的值,下列说法正确的是
| A.常温常压下,6.4g O2和O3的混合气体中含有的分子数为0.4 NA |
| B.标准状况下,2.24 L CCl4分子中共价键的数目为0.4NA |
| C.25℃时,pH=13的Ba(OH)2溶液中含有氢氧根离子数为0.1 NA |
| D.高温下,16.8 g Fe与足量水蒸气完全反应失去0.8NA个电子 |
下列装置适用于实验室制氨气并验证氨气的某化学性质,其中能达到实验目的的是
| A.用装置甲制取氨气 | B.用装置乙除去氨气中的水蒸气 |
| C.用装置丙验证氨气具有还原性 | D.用装置丁吸收尾气 |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.含大量Fe3+的溶液中:Na+、Mg2+、SO42—、SCN— |
B. =106的溶液中:NH4+、K+、AlO2—、NO3— =106的溶液中:NH4+、K+、AlO2—、NO3— |
| C.能使甲基橙变红的溶液中:Cu2+、Mg2+、SO42—、Cl— |
| D.1.0 mol·L—1的KNO3溶液中:Fe2+、H+、Cl—、I— |
下列有关化学用语表示正确的是
A.Al3+的结构示意图: |
B.NaClO的电子式: |
C. 的名称:2—甲基乙醇 的名称:2—甲基乙醇  |
D.乙醛分子的比例模型:  |
为建设“蓝天常在、青山常在、绿水常在”的美丽中国,2015年4月16日国务院颁布了《水污染防治行动计划》。下列做法有利于该目标实现的是
| A.推广使用含磷洗涤剂 |
| B.用O3替代Cl2作饮用水消毒剂 |
| C.用工业污水直接灌溉农田 |
| D.含H2SO4的废水用BaCl2处理后排放 |