已知下列热化学方程式,则③中的Q3值为
Zn(s)+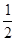 O2(g)= ZnO (s) △H=" -" Q1 kJ• mol-1 ①
O2(g)= ZnO (s) △H=" -" Q1 kJ• mol-1 ①
Hg(l) +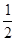 O2(g)= HgO (s) △H= -Q2 kJ• mol-1 ②
O2(g)= HgO (s) △H= -Q2 kJ• mol-1 ②
Zn(s) +HgO (s) = Hg(l)+ ZnO (s) △H= -Q3 kJ• mol-1 ③
| A.Q2 -Q1 | B.Q1 +Q2 | C.Q1- Q2 | D.-Q1- Q2 |
(原创)除去下列物质中的杂质选用的试剂和方法最合理的是
| 物质 |
杂质 |
试剂 |
方法 |
|
| A |
二氧化碳 |
二氧化硫 |
NaOH溶液 |
洗气 |
| B |
氯化亚铁溶液 |
氯化铁 |
过量铁粉 |
过滤 |
| C |
氧化铁 |
氧化铝 |
氨水 |
过滤 |
| D |
氯化钠溶液 |
碘化钠 |
四氯化碳 |
萃取 |
下列有关物质的性质或应用正确的是
| A.实验室常用铝盐溶液与氢氧化钠溶液制备Al(OH)3沉淀 |
| B.浓硫酸能干燥SO2、NO2等气体,说明浓硫酸具有吸水性 |
| C.SO2具有漂白性,通入紫色石蕊溶液中能使溶液先变红后褪色 |
| D.30%的H2O2溶液中加入MnO2可制得O2,MnO2做氧化剂 |
(原创)下列离子方程式书写正确的是
A.实验室用MnO2和浓盐酸制取Cl2:MnO2+4HCl(浓)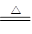 Mn2++2Cl-+Cl2↑+2H2O Mn2++2Cl-+Cl2↑+2H2O |
| B.向NaHSO4溶液中滴加Ba(OH)2溶液至中性:SO42-+2H++Ba2++2OH-=BaSO4↓+2H2O |
| C.漂白粉溶液吸收二氧化碳:Ca2++CO2+H2O=CaCO3↓+2H+ |
D.NH4Cl浓溶液中滴加浓NaOH溶液并加热:NH4++OH-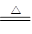 NH3↑+H2O NH3↑+H2O |
(原创)下列各组离子中,在给定条件下能够大量共存的是
| A.在加入铝粉能产生H2的溶液中:NH、Fe2+、SO、NO |
| B.无色碱性溶液中:Na+、K+、MnO4-、CO32- |
| C.c(H+)/c(OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl- |
| D.c(ClO-)= 1.0 mol·L-1的溶液:Na+、SO32-、S2-、SO42- |
下列实验操作与对应的反应现象或原理正确的一组是
| 选项 |
实验操作 |
现象或原理 |
| A |
取少量KI溶液,先滴加氯水,再加入少量苯,振荡、静置 |
溶液分层,下层呈紫红色 |
| B |
将稀盐酸或氢氧化钠溶液慢慢滴入氢氧化铝胶体中 |
均先沉淀后溶解 |
| C |
将浓硝酸加入盛有铂、金的烧杯中,不反应,加入一定量 浓盐酸后,铂、金溶解 |
浓盐酸氧化性强于浓硝酸 |
| D |
将40.0 g NaOH固体溶于1.0 L蒸馏水中配成溶液 |
溶液物质的量浓度为1.0mol·L-1 |