PbO2是褐色固体,受热分解为Pb的+4和+2价的混合氧化物,+4价的Pb能氧化浓盐酸生成Cl2;现将1 mol PbO2加热分解得到O2,向剩余固体中加入足量的浓盐酸得到Cl2,O2和Cl2的物质的量之比为3:2,则剩余固体的组成及物质的量比是( )
| A.2:1混合的Pb3O4、PbO |
| B.1:2混合的PbO2、Pb3O4 |
| C.1:4:1混合的PbO2、Pb3O4、PbO |
| D.1:1:4混合的PbO2、Pb3O4、PbO |
已知气体的摩尔质量越小,扩散速度越快。下图所示为气体扩散速度的实验,两种气体扩散相遇时形成白色烟环。下列关于甲、乙的判断正确的是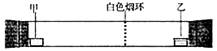
| A.甲是浓氨水,乙是浓硫酸 | B.甲是浓盐酸,乙是浓氨水 |
| C.甲是浓氨水,乙是浓盐酸 | D.甲是浓硝酸,乙是浓氨水 |
一定条件下,将等体积NO和O2充入一试管,并将试管倒立于水槽中,充分反应后剩余气体的体积约为原总体积的
| A.1/8 | B.1/4 | C.3/8 | D.3/4 |
下列递变规律正确的是
| A.HClO4、H2SO4、H3PO4的酸性依次增强 | B.HCl、HBr 、HI的稳定性依次增强 |
| C.钠、镁、铝的金属性依次减弱 | D.N、O、F原子半径逐渐增大 |
如图所示是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是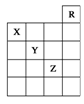
①X的气态氢化物与Y的最高价氧化物对应的水化物能发生反应生成盐。②Y、Z的气态氢化物的水溶液的酸性:Y<Z。③Z的单质在常温下是液体,可与铁粉反应。④Z的原子序数比Y的大19。⑤Z所在的周期中含有32种元素
| A.①②③④ | B.①②③④⑤ | C.只有③ | D.只有①③⑤ |
下列表示物质结构的化学用语或模型正确的是
| A.8个中子的碳原子的符号:14C | B.N2的电子式∶N∶∶∶N∶ |
C.Cl-离子的结构示意图: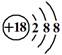 |
D.HF的电子式:H+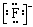 |