下列离子方程式正确的是
| A.向Ca(OH)2溶液中通入过量CO2:Ca2++2OH—+CO2=CaCO3↓+H2O |
| B.将盐酸溶液滴加到石灰石中:CO32—+2H+=CO2↑+H2O |
| C.将少量H2SO4溶液滴加到Ba(OH)2溶液中:2H++SO42—+2OH—+Ba2+=BaSO4↓+2H2O |
| D.将铁粉加入到AgNO3溶液中:Fe+Ag+=Ag+Fe2+ |
含有一定量NaOH溶液中,逐渐通入一定量 CO2,充分反应后,将溶液在一定条件下进行蒸干,得到晶体物质。其质量m 与通入气体体积V(CO2)的关系如图。如下说法正确的是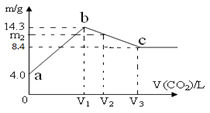
| A.晶体物质:a点是NaOH;b点是Na2CO3;c点是NaHCO3 |
| B.a→b 和 b→c 两段过程得到的晶体,含有相同的晶体物质 |
| C.整个过程中的溶液,一定存在恒等式:c(Na+)+c(H+)=c(OH-)+c(CO32-)+c(HCO3-) |
| D.若通入V2=1.344 L (标况) 气体,则m2=13.12 g |
能正确表示下列各组溶液混合后,所得液体恰好呈中性的离子方程式是
| A.Ba(OH)2和NaHSO4:Ba2+ +2OH— +2H+ +SO42—→BaSO4↓+ 2H2O |
| B.Ba(OH)2和NaHSO4:Ba2+ + OH—+ H++ SO42—→BaSO4↓+ H2O |
| C.Ba(OH)2和KAl(SO4)2:2Ba2++ 4OH—+ Al3++ 2SO42—→2BaSO4↓+ AlO2— |
| D.Ba(OH)2和KAl(SO4)2:3Ba2+ + 6OH—+ 2Al3++ 3SO42—→3BaSO4↓+2Al(OH)3↓ |
三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生如下反应:
3NF3+5H2O→2NO+HNO3+9HF。下列有关该反应的说法正确的是
| A.NF3是氧化剂,H2O是还原剂 |
| B.NF3是极性分子,在潮湿空气中泄漏会看到红棕色气体 |
| C.若生成1 mol HNO3,则转移2NA个电子 |
| D.每消耗0.2mol氧化剂,可收集到5.418L气体 |
今有一混合物的水溶液,只可能含有以下离子中的若干种:NH4+ 、Cl-、Mg2+、Ba2+、K+、CO32-、SO42-,现取三份100 mL溶液进行如下实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加足量NaOH溶液加热后,收集到气体0.04mol
③第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33 g。
根据上述实验,以下推测正确的是
| A.K+可能存在 | B.该溶液中含CO32-离子的浓度为0.2mol/L |
| C.Cl-一定不存在 | D.Ba2+一定不存在,Mg2+可能存在 |
铜和镁的合金2.3 g完全溶于浓HNO3,若反应中硝酸被还原只产生2.240 L的NO2气体和168 mL的N2O4气体(都已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生产沉淀的质量为
| A.4.1275g | B.4.255 g | C.8.51 g | D.9.62 g |