下列实验误差分析错误的是( )
| A.滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小 |
| B.用容量瓶配置溶液,定容时俯视刻度线,所配溶液浓度偏小 |
| C.用湿润的pH试纸测稀碱液的pH,测定值偏小 |
| D.测定中和反应反的应热时,将碱液缓慢倒入酸中,所测温度值偏小 |
利用如图所示装置可以模拟钢铁的电化学防护。下列说法正确的是
| A.若X为锌棒,开关K置于M处,铁极发生还原反应 |
| B.若X为碳棒,开关K置于N处,X极发生还原反应 |
| C.若X为碳棒,开关K置于N处,可加快铁的腐蚀 |
| D.若X为锌棒,开关K置于M处,可加快铁的腐蚀 |
央视“315特别行动”曝光了河南一些地方“瘦肉精”事件。“瘦肉精”对人体健康会产生危害。已知某种“瘦肉精”含有克伦特罗(Clenbuterol),其结构如下图。下列有关克伦特罗的叙述,正确的是
| A.该物质的分子式为C12H17ON2Cl |
| B.该物质不溶于盐酸 |
| C.该物质能与FeCl3溶液发生显色反应 |
| D.该物质分子间都可以形成氢键 |
结构为 的有机物可以通过不同的反应得到下列四种物质:
的有机物可以通过不同的反应得到下列四种物质:
① ②
② ③
③ ④
④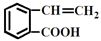
生成这四种有机物的反应类型依次为
| A.酯化、取代、缩聚、取代 | B.取代、取代、加聚、消去 |
| C.取代、缩聚、酯化、消去 | D.取代、加成、酯化、消去 |
氯化钴溶液中存在下列平衡:CoCl42-(蓝色) Co2+(粉红色)+4Cl-,向氯化钴稀溶液中加入一定量的浓盐酸,溶液的颜色变化是
Co2+(粉红色)+4Cl-,向氯化钴稀溶液中加入一定量的浓盐酸,溶液的颜色变化是
| A.由蓝色变为粉红色 | B.红色加深 |
| C.由粉红色变为蓝色 | D.蓝色加深 |
铜锌原电池(如右图)工作时,下列叙述正确的是
| A.在外电路中,电流从Zn极流向Cu极 |
| B.盐桥中的Cl-移向CuSO4溶液 |
| C.当负极减小65g时,正极增加65g |
| D.电池的总反应为 Zn + Cu2+=Zn2+ + Cu |