醋酸是电解质,下列事实都能说明醋酸是弱电解质的组合是( )
①醋酸与水能以任意比互溶 ②醋酸溶液能导电
③醋酸溶液中存在醋酸分子 ④0.1 mol/L醋酸的pH比0.1 mol/L盐酸pH大
⑤醋酸能和碳酸钙反应放出CO2 ⑥常温下0.1 mol/L醋酸钠溶液pH=8.9
⑦大小相同的锌粒与相同物质的量浓度的盐酸和醋酸反应,醋酸产生H2速率慢
| A.②⑥⑦ | B.③④⑤⑥ | C.③④⑥⑦ | D.①② |
下列实验操作正确的是
①用稀硫酸洗涤长期存放石灰水的试剂瓶;
②用带橡胶塞的棕色试剂瓶存放浓硫酸;
③用盐酸酸化过的FeCl3溶液,除去H2还原CuO实验留在试管内的铜;
④测定某溶液的pH时,先用蒸馏水润湿pH试纸,再甩洁净、干燥的玻璃棒蘸取该溶, 液点在试纸上,并与标准比色卡比较;
⑤分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出; ⑥蒸馏时,将温度计的水银球靠近蒸馏烧瓶支管口。
⑥蒸馏时,将温度计的水银球靠近蒸馏烧瓶支管口。
| A.①③ | B.②③④ | C.②③ | D.③⑤⑥ |
CH4催化还原NOx可以消除氮氧化物的污染.例如:
①CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g);ΔH=-574 kJ/mol
②CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g); ΔH=-1160 kJ/mol
ΔH=-1160 kJ/mol
下列说法不正确的是
| A.反应①②均为放热反应 |
B.反应①②转移的电 子数相同 子数相同 |
C. 由反应①可推知:CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(l) ΔH=-a kJ/mol,a<574 由反应①可推知:CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(l) ΔH=-a kJ/mol,a<574 |
| D.若用标准状况下4.48 L CH4通过上述反应还原NO2至N2,放出的热量为173.4kJ |
在一定条件下,在密闭容器中反应:2NO2(g)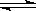 O2(g)+ 2NO(g) ΔH>0,达到
O2(g)+ 2NO(g) ΔH>0,达到 平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是
平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是
| A.当X表示温度时,Y表示NO的物质的量 |
| B.当X表示压强时,Y表示NO2的转化率 |
| C.当X表示反应时间时,Y表示混合气体的密度 |
| D.当X表示NO2的物质的量时,Y表示O2的物质的量 |
已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图所示。下列说法正确的是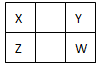
| A.Z元素的原子半径可能比Y元素的小 |
| B.Z的最高价氧化物的水化物的酸性一定比W的强 |
| C.W的气态氢化物的稳定性一定比Y的强 |
| D.Z元素的最高化合价可能比Y元素的高 |
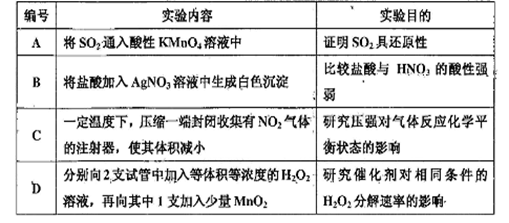
下述实验中,不能达到预期目的的是