下列说法正确的是(NA表示阿伏加德罗常数的值)
| A.常温常压下,18g NH4+所含的电子数为10NA |
| B.56g金属铁与氯气反应时得到的电子数为3NA |
| C.标准状态下,22.4L氧气所含的氧原子数为2 NA |
| D.1 mol由Na2O2和Na2O组成的混合物,其中的钠离子数为4 NA |
在恒容密闭容器中,可以作为2NO2(g)  2NO(g)+O2(g)达到平衡状态的标志是:①单位时间内生成n mol O2的同时生成2n mol NO2;②单位时间内生成n mol O2的同时生成2n mol NO;③混合气体的颜色不再改变;④混合气体的密度不再改变的状态;⑤混合气体的平均相对分子质量不再改变的状态;⑥混合气体中NO与O2的物质的量之比保持恒定;⑦混合气体中NO与NO2的物质的量之比保持恒定
2NO(g)+O2(g)达到平衡状态的标志是:①单位时间内生成n mol O2的同时生成2n mol NO2;②单位时间内生成n mol O2的同时生成2n mol NO;③混合气体的颜色不再改变;④混合气体的密度不再改变的状态;⑤混合气体的平均相对分子质量不再改变的状态;⑥混合气体中NO与O2的物质的量之比保持恒定;⑦混合气体中NO与NO2的物质的量之比保持恒定
A ①③⑤⑦B.②④⑤C.①③④D.①②③④⑤
右图是关于反应A2(g)+3B2(g) 2C(g)ΔH<0的平衡移动图像,影响平衡移动的原因是
2C(g)ΔH<0的平衡移动图像,影响平衡移动的原因是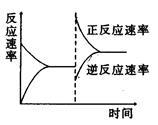
| A.升高温度,同时加压 |
| B.降低温度,同时减压 |
| C.增大反应物浓度,同时使用催化剂 |
| D.增大反应物浓度,同时减小生成物浓度 |
纳米钴(Co)加氢反应的催化剂,500K时催化反应:CO(g)+3H2(g )  CH4(g)+H2O(g) △H<0。有关说法正确的是
CH4(g)+H2O(g) △H<0。有关说法正确的是
| A.纳米技术的应用,提高了催化剂的催化性能,但平衡常数不变 |
| B.缩小容器体积,平衡向正反应方向移动CO的浓度减小 |
| C.温度越低,越有利于CO催化加氢 |
| D.从平衡体系中分H2O(g)能加快正反应速率 |
工业上常利用CO与SO2反应生成固态S单质和CO2,从而消除这两种气体对大气的污染:2CO(g)+SO2(g) 2CO2(g)+S(s)△H=﹣a kJ/mol(a>0),下列叙述正确的是
2CO2(g)+S(s)△H=﹣a kJ/mol(a>0),下列叙述正确的是
A.该反应的平衡常数表达式为K=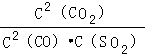 |
| B.若反应开始时投入2 mol CO,则达平衡时,放出热量为a kJ |
| C.增大压强或升高温度都可以加快化学反应速率并提高SO2的转化率 |
| D.若单位时间内生成2 molCO2的同时,消耗1mol SO2,则说明反应达到平衡状态 |
已知:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=﹣49.0kJ·mol﹣1.一定条件下,向体积为1L的密闭容器中充入1mol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间的变化曲线如图所示,下列叙述中正确的是
CH3OH(g)+H2O(g)△H=﹣49.0kJ·mol﹣1.一定条件下,向体积为1L的密闭容器中充入1mol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间的变化曲线如图所示,下列叙述中正确的是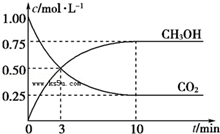
| A.欲增大平衡状态时c(CH3OH)/c(CO2)的比值, 可采用 升高温度的方法 |
| B.3 min时,CO2的消耗速率等于CH3OH的生成速率,且二者浓度相同 |
| C.欲提高H2的平衡转化率只能减小反应容器的体积 |
| D.从反应开始到平衡,CO2的平均反应速率v(CO2)="0.025" mol·L﹣1·min﹣1 |