在相同条件下的三个反应: 2A- +B2 =2B- +A2; 2C- +A2 =2A- +C2; 2B- +D2 =2D- +B2,下列判断不正确的是( )
| A.氧化性: B2> A2 | B.还原性: C- > D- |
| C.2A- +D2 =2D- + A2反应可以进行 | D.2C- +B2 =2B- + C2反应不能进行 |
有关离子浓度大小比较的判断正确的是
| A.往醋酸中滴加氢氧化钠溶液到溶液呈中性,c(Na+)=c(CH3COO-) |
| B.Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| C.KHSO3溶液呈酸性,c(K+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-) |
| D.0.1mol/L的NH4Cl溶液中,c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
4种相邻主族短周期元素的相对位置如表,元素X的原子核外电子数是M的2倍,Y的氧化物具有两性。回答下列问题
| M |
N |
||
| X |
Y |
A.金属性:X<Y
B.氢化物的稳定性:M>N
C.M是自然界中化合物最多的元素
D.N与Y的最高价氧化物的水化物能相互反应
如图为示意图,下列说法正确的是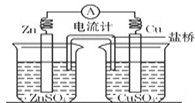
| A.电子从锌片流向铜片 |
| B.若以含氯化钾的琼脂作盐桥,则氯离子定向移动到右边的烧杯 |
| C.铜片逐渐溶解,发生氧化反应 |
| D.该装置是将电能转变为化学能的装置 |
下列实验操作或装置符合实验要求的是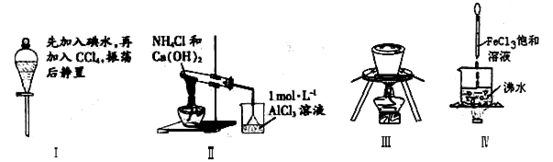
| A.实验Ⅰ:液体分层,下层呈无色 |
| B.实验Ⅱ:烧杯中先出现白色沉淀,后溶解 |
| C.装置III可用于高温煅烧石灰石 |
| D.实验IV:继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应 |
下列陈述Ⅰ、Ⅱ错误或因果关系不成立的是
| 选项 |
陈述Ⅰ |
陈述Ⅱ |
| A |
某吸热反应能自发进行 |
该反应是熵增反应 |
| B |
NH4F水溶液中含有HF |
NH4F溶液不能存放于玻璃试剂瓶中 |
| C |
常温下浓硫酸存放在铝制的器皿中 |
浓硫酸不与铝反应 |
| D |
氢氧化铝可作胃酸的中和剂 |
氢氧化铝是两性氢氧化物 |