下列条件下,两瓶气体所含原子数一定相等的是( )
| A.同质量的C2H4和CO | B.同体积、同密度的C2 H4和C3 H6 |
| C.同温度、同体积的H2和N2 | D.同压强、同体积的N2 O和CO2 |
下列说法或表示方法正确的是
| A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B.由H+(aq)+OH-(aq)===H2O(l)△H=-57.3kJ·mol-1可知,若将含1 mol CH3COOH的稀溶液与含1 mol NaOH的稀溶液混合,放出的热量小于57.3 kJ |
| C.由C(石墨)="=" C(金刚石)△H= +1.90 kJ·mol-1可知,金刚石比石墨稳定 |
D.500℃、30MPa下,将0.5molN2(g)和1.5mol H2(g)置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g)△H=-38.6kJ·mol-1 2NH3(g)△H=-38.6kJ·mol-1 |
将mg钠和铝的混合物放入ng水中,待反应停止后,得到ag沉淀,则滤液中的溶质是
| A.NaAlO2 | B.NaAlO2和NaOH | C.Al(OH)3 | D.NaOH |
铜和镁的合金4.6 g完全溶于浓硝酸,若反应中硝酸被还原只产生5.152L的NO2气体(已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为
| A.9.02 g | B.8.51 g | C.8.26 g | D.7.04 g |
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如下图所示。则下列有关说法中,不正确的是
| A.还原性:I— >Fe2+>Br— |
| B.原混合溶液中FeBr2的物质的量为6mol |
| C.当通入2molCl2时,溶液中已发生的离子反应可表示为: 2Fe2++2I-+2Cl2===2Fe3++I2+4Cl- |
| D.原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3 |
在下列物质转化关系中,反应的条件和部分产物已略去。已知甲、乙是两种常见金属,甲的焰色反应呈黄色,乙与H2O需要在高温下反应,反应Ⅲ是工业制盐酸的反应,则下列说法正确的是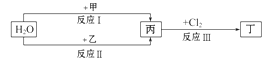
| A.工业上生产甲可以用热还原法 |
| B.反应Ⅱ的另外一种产物具有磁性 |
| C.向乙与Cl2反应产物的溶液中滴加KSCN溶液,无明显现象 |
| D.当有1mol乙参加反应Ⅱ时转移8mol电子 |