下列关于电解质溶液的叙述正确的是
| A.常温下,同浓度的Na2CO3与NaHCO3溶液相比,Na2CO3溶液的pH大 |
| B.常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Clˉ)>c(NH4+)>c(H+)=c(OHˉ) |
| C.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 |
| D.将pH = 4的盐酸稀释后,溶液中所有离子的浓度均降低 |
下列化合物中,在常温常压下以液态形式存在的是()
| A.甲醇 | B.新戊烷 | C.丁烯 | D.丁烷 |
下列反应中,属于取代反应的是()
①CH3CH=CH2+Br2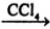 CH3CHBrCH2Br
CH3CHBrCH2Br
②CH3CH2OH 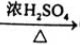 CH2=CH2+H2O
CH2=CH2+H2O
③CH3COOH+CH3CH2OH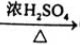 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
④C6H6+HNO3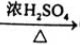 C6H5NO2+H2O
C6H5NO2+H2O
| A.①② | B.③④ | C.①③ | D.②④ |
分子式为C5H11Cl的同分异构体共有(不考虑立体异构)。()
| A.6种 | B.7种 | C.8种 | D.9种 |
分子式为C10H14的单取代芳烃,其可能的结构有()
| A.2种 | B.3种 | C.4种 | D.5种 |
下列物质中存在顺反异构体的是 ( )
| A. 2-氯丙烯 | B.丙烯 | C. 2-丁烯 | D. 1-丁烯 |