月球上含有丰富的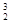 He。关于
He。关于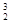 He的说法不正确的是
He的说法不正确的是
| A.是一种核素 | B.原子核内有1个中子 |
C.与 He互为同位素 He互为同位素 |
D.比 He少一个电子 He少一个电子 |
下列化合物,按其晶体的熔点由高到低排列正确的是
| A.SiO2 CsCl CBr4CF4 | B.SiO2CsCl CF4CBr4 |
| C.CsCl SiO2 CBr4CF4 | D.CF4CBr4CsCl SiO2 |
某氧化剂中,起氧化作用的是X2O72-离子,在溶液中0.2 mol该离子恰好能使0.6molSO32-离子完全氧化,则X2O72-离子还原后的化合价为()。
| A.+1 | B.+2 | C.+3 | D.+4 |
在2KMnO4+16HCl====2KCl+2MnCl2+5Cl2↑+8H2O的反应中,氧化剂和还原剂的物质的量之比为
| A.1∶8 | B.8∶1 | C.1∶5 | D.5∶1 |
实验室配制1mol·L-1盐酸250mL,下列不需用的仪是:
| A.250ml容量瓶 | B.托盘天平 | C.胶头滴管 | D.烧杯 |
NA表示阿伏加德罗常数,下列叙述正确的是
| A.等物质的量的N2和CO所含分子数均为NA |
| B.1.7g H2O2中含有的电子数为0.9 NA |
| C.1mol Na2O2固体中含离子总数为4 NA |
| D.标准状况下,2.24L戊烷所含分子数为0.1 NA |