下列关于C、Si、S、Cl四种非金属元素的说法中,正确的是( )
A.两两结合形成的化合物都是共价化合物
B.在自然界中都能以游离态存在
C.氢化物的热稳定性比较:CH4<SiH4<H2S<HCl
D.最高价氧化物都能与水反应生成相应的酸,且酸性依次增强
相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:
X2(g)+3Y2(g) 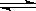 2XY3(g) ΔH=-92.6 kJ·mol-1实验测得反应在起始、达到平衡时的有关数据如下表所示:下列叙述不正确的是( )
2XY3(g) ΔH=-92.6 kJ·mol-1实验测得反应在起始、达到平衡时的有关数据如下表所示:下列叙述不正确的是( )
| 容器编号 |
起始时各物质物质的量(mol) |
达平衡时体系能量的变化 |
||
| X2 |
Y2 |
XY3 |
||
| ① |
1 |
3 |
0 |
放热 23.15 kJ |
| ② |
0.6 |
1.8 |
0.8 |
Q (Q>0) |
A.容器①、②中反应的平衡常数相等
B.达平衡时,两个容器中XY3的物质的量浓度均为2 mol·L-1
C.容器②中反应达到平衡时放出的热量为Q
D.若容器①体积为0.20 L,则达平衡时放出的热量大于23.15 kJ
将一定量的固体Ag2SO4置于容积不变的密闭容器中(装有少量V2O5),某温度下发生反应:Ag2SO4(s)  Ag2O(s)+SO3(g),2 SO3(g)
Ag2O(s)+SO3(g),2 SO3(g)  2 SO2(g)+ O2(g),反应经过10 min达到平衡,测得c(SO3)=0.4mol/L,c(SO2)=0.1mol/L,则下列叙述中不正确的是( )
2 SO2(g)+ O2(g),反应经过10 min达到平衡,测得c(SO3)=0.4mol/L,c(SO2)=0.1mol/L,则下列叙述中不正确的是( )
| A.这10 min内氧气的平均反应速率为0.005 mol·mol-1·min-1 |
| B.SO3的分解率为20% |
| C.容器里气体的密度为40g/L |
| D.硫酸银与三氧化硫的化学反应速率相同 |
如图所示,甲容器容积固定不变,乙容器有可移动的活塞。甲中充入2 mol SO2和1mol O2,乙中充入4 mol SO3和1mol He,在恒定温度和相同的催化剂条件下,发生如下反应:2SO3(g)  2SO2(g)+ O2 (g)下列有关说法正确的是
2SO2(g)+ O2 (g)下列有关说法正确的是
| A.若活塞固定在6处不动,达平衡时甲乙两容器中的压强:P乙=P甲 |
| B.若活塞固定在3处不动,达平衡时甲乙两容器中SO3的浓度: c(SO3)乙>2c(SO3)甲 |
| C.若活塞固定在3处不动,达平衡时甲乙容两器中SO2的体积分数:ψ(SO2)乙>2ψ(SO2)甲 |
| D.若活塞固定在7处不动,达平衡时两容器中SO3的物质的量分数相等 |
已建立化学平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,下列有关叙述正确的是
①生成物的百分含量一定增加②生成物的产量一定增加③反应物的转化率一定增大
④反应物浓度一定降低⑤正反应速率一定大于逆反应速率 ⑥使用了合适催化剂
| A.②⑤ | B.①② | C.③⑤ | D.④⑥ |
常温下0.1mol/L碳酸溶液中,下列离子关系式正确的是
| A.c(H+)="2" c(CO32-)+c(OH-) |
| B.0.1= c(HCO3-)+2c(CO32-) |
| C.c(OH-)= c(H+) - c(HCO3-)-2 c(CO32-) |
| D.c(H+)>c(CO32-) > c(HCO3-) |