下列离子方程式正确的是
| A.氨水吸收足量的SO2气体:OH-+SO2=HSO3- |
| B.将铜丝投入稀硝酸中:Cu+4H++NO3-=Cu2++NO2↑+2H2O |
| C.将H2O2滴入酸性KMnO4溶液中:2MnO4-+10H++3H2O2=2Mn2++3O2↑+8H2O |
| D.NaHSO4溶液中加入过量Ba(OH)2溶液:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
下列物质属于电解质的是
| A.石墨 | B.烧碱 | C.蔗糖 | D.金属铝 |
取一定物质的量浓度的NaOH溶液100mL,然后向其通入一定量的CO2气体,得到溶液A,向A中逐滴缓慢加入0.1mol/L的HCl溶液,产生的CO2气体体积(标准状况)与所加
HCl溶液的体积之间关系如图所示,下列有关说法不正确的是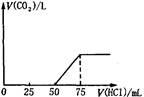
| A.A溶液中溶质Na2CO3和NaHCO3物质的量比为1:1 |
| B.A溶液中溶质NaOH和Na2CO3物质的量比为1:1 |
| C.原NaOH溶液物质的量浓度为0.075mol/L |
| D.通入CO2气体在标况下的体积为56mL |
在加入酚酞变红色的无色溶液中,下列各组离子能够大量共存的是()
| A.NH4+、Na+、Cl-、SO42- | B.MnO4-、K+、NO3-、SO42- |
| C.Ag+、NO3-、I-、H+ | D.ClO-、Na+、NO3-、K+ |
2H2O2=2H2O+O2 2KClO3=2KCl+3O2 2HgO=2Hg+O2 2Na2O2+2CO2=2Na2CO3+O2,
现要制备等量的O2,则转移的电子数之比为()
| A.1:1:1:1 | B.1:2:2:1 | C.2:1:1:2 | D.1:2:1:2 |
氯化碘(ICl)的化学性质跟Cl2相似,预计它与H2O反应的最初生成物是
| A.HI和HClO | B.HCl和HIO | C.HClO3和HIO | D.HCl和HI |