500mLNH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含amol氢氧化钠的溶液恰好反应完全;另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为
| A.(l0b - 5a) mol/L | B.(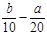 )mol/L )mol/L |
C.(5b一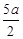 )mol/L )mol/L |
D.(2b—a)mol/L |
下列化学反应的离子方程式错误的是()
| A.Al(OH)3与盐酸反应: Al(OH)3+3H+===Al3++3H2O |
| B.Al2O3溶于过量NaOH溶液: Al2O3+2OH-===2AlO+H2O |
| C.铁溶于稀H2SO4∶Fe+2H+===Fe2++H2↑ |
| D.Al(OH)3溶于NaOH溶液: Al(OH)3+3OH-===AlO+3H2O |
下列观点你认为正确的是()
| A.某单质固体能导电,该单质一定是金属 |
| B.某化合物的水溶液能导电,该化合物一定是电解质 |
| C.纯水的导电性很差,所以水不是电解质 |
| D.Na2O液态时能导电,所以Na2O是电解质 |
金属钠着火时,可以灭火的物质是()。
| A.水 | B.砂子 | C.煤油 | D. 二氧化碳 二氧化碳 |
下列物质中,既能与稀硫酸反应,又能与氢氧化钠溶液反应的是
2molNa2O2与5molNaHCO3固体混合后,在密闭容器中加热充分反应后,排出气体后冷却,残留的固体物质是
| A.Na2CO3 | B.Na2O2、Na2CO3 |
| C.NaOH、Na2CO3 | D.NaOH、Na2O2、Na2CO3 |