电化学在日常生活中用途广泛,图①是镁一次氯酸钠燃料电池,电池总反应为:
Mg+ClO—+H2O= Cl—+ Mg(OH)2↓,图②是Cr2O2—7的工业废水的处理。下列说法正确的是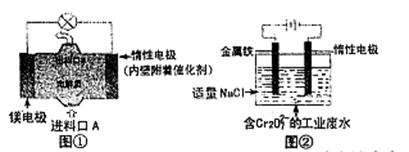
| A.图②中Cr2O2—7离子向惰性电极移动,与该极附近的OH—结合转化成Cr(OH)3除去 |
| B.图②的电解池中,有0.084 g阳极材料参与反应,阴极会有336 mL的气体产生 |
| C.图①中发生的还原反应是:Mg2++ClO—+ H2O+ 2e—=Cl—+ Mg(OH)2↓ |
| D.若图①中3.6 g镁溶解产生的电量用以图②废水处理,理论可产生10.7 g氢氧化铁沉淀 |
用下列实验装置完成对应的实验,能达到实验目的的是
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色呈黄色。五种元素核电荷数之和为54,最外层电子数之和为20。W、Z是同主族元素,Z的核电荷数是W的2倍。工业上一般通过电解氧化物的方法获得Y单质。则下列说法不正确的是
| A.原子半径:X>Y>Q>W |
| B.X、Y和W三种元素形成化合物的水溶液呈碱性 |
| C.W的氢化物的稳定性比Z强 |
| D.Q和W可形成原子个数比为1∶1和2∶1的化合物 |
下列有关物质的性质或应用的说法中正确的是
| A.石油的催化裂化及裂解可以得到较多的轻质油和气态烯烃 |
| B.Si是一种非金属主族元素,其氧化物可用于制作计算机芯片 |
| C.Mg、Fe等金属在一定条件下与水反应都生成H2和对应的氢氧化物 |
| D.蛋白质溶液中加入浓的硫酸钠溶液,有沉淀析出,这种作用称为变性。 |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.8.4gNaHCO3固体中含HCO3−数目为0.1NA |
| B.60g 二氧化硅中含Si-O键2NA |
| C.1molN2和3molH2合成氨,生成的NH3分子数为2NA |
| D.1 mol氯气与氢氧化钙完全反应生成氯化钙和次氯酸钙,转移的电子数为2NA |
在下列各溶液中,离子一定能大量共存的是
| A.能使紫色石蕊试液变红的溶液中:Fe2+、Na+、SO42-、NO3- |
| B.c(H+)∶c(OH-)=1∶2的水溶液中:Na+、K+、NO3-、ClO- |
| C.水电离出的c(H+)=10-12mol/L中:Na+、Cu2+、Cl-、S2- |
| D.加入Al能放出氢气的溶液中:NH4+、SO42-、Cl-、ClO- |