(1)已知:①Fe(s)+1/2O2(g)=FeO(s) △H1=-272.0KJ·mol-1
②2Al(s)+3/2(g)=Al2O3(s) △H2=-1675.7KJ·mol-1
Al和FeO发生铝热反应的热化学方程式是__ __。
某同学认为,铝热反应可用于工业炼铁,你的判断是_ (填“能”或“不能”),你的理由 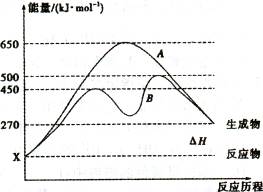
(2)反应物与生成物均为气态的某可逆反应在不同条件下的反应历程分别为A.B,如图所示。①据图判断该反应是 (填“吸”或“放” )热反应,当反应达到平衡后,其他条件不变,,升高温度,反应物的转化率将 (填“增大”、 “减小”或“不变”)。
②其中B历程表明此反应采用的条件为
(填字母)。
A.升高温度 B.增大反应物的浓度
C.降低温度 D.使用催化剂
2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示,已知1 mol SO2(g)被为1 mol SO3(g)的ΔH=-99 kJ/mol。
2SO3(g)反应过程的能量变化如图所示,已知1 mol SO2(g)被为1 mol SO3(g)的ΔH=-99 kJ/mol。
回答下列问题:
(1)图中A、C分别表示:_________________、__________________;E的大小对该反应的反应热有无影响?_______________________;该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?_____________;理由是_______________________。
(2)图中ΔH=______________
(3)V2O5的催化物质循环机理可能为:V2O5氧化SO2时,自己被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:___________________。
(4)已知单质硫的燃烧热为296 kJ/mol,计算由S(g)生成3 mol SO3(g)的ΔH=____________
(1)2,4,6三甲基5乙基辛烷的分子中共有________个甲基。
(2)分子中有6个甲基且一溴代物只有1种的烷烃的结构简式是_______________,名称是_________。
(3)通过乙炔制备氯乙烯______________________________。
(4)2-氯丙烷与KOH的乙醇溶液共热___________________________。
(5)甲苯在铁粉催化下与溴单质生成一溴代物_________________________。
在如图所示的装置中,若通直流电5min时,铜电极质量增加2.16 g。试回答下列问题。
(1)电源中X电极为直流电源的________极。
(2)pH变化:A:________,B:________,C:________。(填“增大”、“减小”或“不变”)
(3)通电5 min时,B中共收集224 mL (标准状况下) 气体,溶液体积为200 mL,则通电前CuSO4溶液的物质的量浓度为________(假设电解前后溶液体积无变化)。
(4)若A中KCl足量且溶液的体积也是200 mL,电解后,溶液的pH为________(假设电解前后溶液体积无变化)。
已知25 ℃时有关弱酸的电离平衡常数:
| 弱酸化学式 |
HSCN |
CH3COOH |
HCN |
H2CO3 |
| 电离平衡常数 |
1.3×10—1 |
1.8×10—5 |
4.9×10—10 |
K1=4.3×10—7 K2=5.6×10—11 |
(1)同温度下,等pH值的a.NaHCO3 b.NaCN c.Na2CO3溶液的物质的量浓度由大到小的顺序为_____________(填序号)。
(2)25℃时,将20mL 0.1mol·L-1 CH3COOH溶液和20mL 0.1mol·L-1 HSCN溶液分别与20mL 0.1 mol·L-1 NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示:
反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是:______________________。
反应结束后所得两溶液中,c(SCN—) c(CH3COO—)(填“>”、“<”或“=”)
(3)若保持温度不变,在醋酸溶液中加入一定量氨气,下列量会变小的是______________(填序号)
a.c(CH3COO-) b.c(H+) c.KW d.醋酸电离平衡常数
(1)在0.10 mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)= mol·L-1(Ksp[Cu(OH)2]=2.2×10-20)。若在0.1 mol·L-1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是 mol·L-1。
(2)Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s) Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5 mol/L时,溶液的pH应调至 。
Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5 mol/L时,溶液的pH应调至 。
(3)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液是 (填“酸”、“碱”或“中”)性;用含a的代数式表示NH3·H2O的电离常数Kb= 。