下列关于有机物的叙述正确的是
| A.乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别 |
| B.除去乙烷中少量的乙烯,可在光照条件下通入Cl2,再气液分离 |
| C.乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 |
| D.蛋白质、葡萄糖、油脂均能发生水解反应 |
向100mL18mol/L的硫酸中加入足量铜片,加热并充分反应.下列有关说法正确的是( )
| A.充分反应后转移1.8mol电子 | B.H2SO4只作氧化剂 |
| C.若不加热应生成H2 | D.消耗的铜的质量一定少于57.6g |
酸有广泛的用途,下列关于硝酸的叙述中,正确的是( )
| A.溶有二氧化氮的浓硝酸可作火箭中的助燃剂 |
| B.现代工业中使用硝酸钠与浓硫酸反应制取硝酸 |
| C.稀硝酸与铜反应生成NO,浓硝酸与铜反应则生成NO2,说明稀硝酸的氧化性更强 |
| D.稀硝酸具有酸性,可与硫化亚铁反应生成硫化氢气体 |
如图为反应2H2(g)+O2(g) 2H2O(g)的能量变化示意图。下列说法正确的是
2H2O(g)的能量变化示意图。下列说法正确的是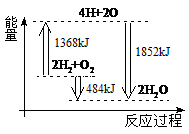
| A.拆开2 mol H2(g)和1 mol O2(g)中的化学键成为H、O原子,共放出1368 kJ能量 |
| B.由H、O原子形成2 mol H2O(g),共吸收1852 kJ能量 |
| C.2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(l),共吸收484 kJ能量 |
| D.2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(g),共放出484 kJ能量 |
下列叙述中正确的是( )
| A.氯水、二氧化硫、活性炭的漂白或脱色原理虽然不同,但它们都能使品红或墨迹褪色。 |
| B.等物质的量的Cl2和SO2同时与潮湿的红布条作用,红布条立即褪色。 |
| C.反应CuSO4+H2S=CuS↓+H2SO4能进行,说明硫化铜既不溶于水,也不溶于稀硫酸。 |
| D.经Cl2和SO2漂白的物质,日后都会恢复原来的颜色。 |
从经济效益和环境保护考虑,大量制取硝酸铜最宜采用的方法是()
| A.Cu + HNO3(浓)→ Cu(NO3)2 |
| B.Cu + HNO3(稀)→ Cu(NO3)2 |
C.Cu  CuO CuO  Cu(NO3)2 Cu(NO3)2 |
| D.Cu + AgNO3 →Cu(NO3)2 |