化合物A、B、C、D各由两种元素组成,甲、乙、丙是短周期元素的三种单质。这些常见的化合物与单质之间存在如下关系(已知C是一种有机物),以下结论不正确的( )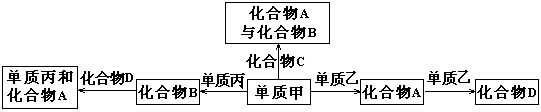
A.常温下,化合物A、B、C、D均为气体
B.上图所示的五个转化关系中,有三个是化合反应
C.上图所示的五个转化关系中,均为氧化还原反应
D.上述转化关系所涉及的化合物中只有一种是电解质
在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是C
| A.Na+、K+、Cl-HCO3-、 | B.Na+、Cu2+、SO42-、NO3- |
| C.Mg2+、NH4+、SO42-、Cl- | D.Ba2+、Fe2+、NO3-、K+ |
用稀硫酸与铁片反应制取氢气时,下列措施不能使氢气生成速率增大的是
| A.给反应体系适当加热 | B.向反应体系中加水稀释 |
| C.向反应体系中加入少量氧化铜固体 | D.将铁片换成铁粉 |
限用一种试剂, 经过一次性实验就能鉴别下列四种溶液:Na2CO3、(NH4)2SO4、NH4Cl、KNO3, 应选用:
| A.AgNO3溶液 | B.NaOH溶液 |
| C.Ba(OH)2溶液 | D.盐酸 |
对于下列事实的解释错误的是
| A.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 |
| B.浓硝酸在光照下颜色变黄,说明浓硝酸不稳定 |
| C.常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应 |
| D.氨水可使酚酞试剂变为红色,说明氨溶解于水显弱碱性 |
有关化学用语正确的
| A.次氯酸的电子式:H ∶Cl∶O∶ | B.二氧化硅的分子式:SiO2 |
| C.氮气的结构式:∶N≡N∶ | D.氯化镁的电子式: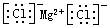 |