“拟晶”(quasicrystal)是一种具有凸多面体规则外形但不同于晶体的固态物质。A165Cu23Fel2是二十世纪发现的几百种拟晶之一,具有合金的某些优良物理性能。有关这种拟晶的说法错误的是:
| A.A165Cu23Fel2的硬度比金属A1、Cu、Fe都大 |
| B.A165Cu23Fel2中三种金属的化合价均可视作零 |
| C.A165Cu23Fel2不可用作长期浸泡在海水中的材料 |
| D.1mol A165Cu23Fel2溶于过量的硝酸时共失去265 mol电子 |
反应①是自海藻灰中提取碘的主要反应,反应②是自智利硝石中提取碘的主要反应:①2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2;
②2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2。已知NaIO3的氧化性与MnO2相近,下列有关说法正确的是
| A.两个反应中生成等量的I2时转移的电子数相等 |
| B.I2在反应①②中都是氧化产物 |
| C.NaI和NaIO3在一定条件下能反应生成I2 |
| D.NaIO3在任何化学反应中只能作氧化剂,不能作还原剂 |
固定和利用CO2,能有效地利用资源,并减少空气中的温室气体。工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol,某科学实验将6 mol CO2和8 mol H2充入一容积为2 L的密闭容器中,测得H2的物质的量随时间变化如图中实线所示(图中字母后数字表示对应的坐标):下列说法不正确的是
CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol,某科学实验将6 mol CO2和8 mol H2充入一容积为2 L的密闭容器中,测得H2的物质的量随时间变化如图中实线所示(图中字母后数字表示对应的坐标):下列说法不正确的是
| A.该反应在低温条件下能自发进行 |
| B.曲线Ⅰ改变的条件可能是升高温度 |
| C.若实线对应条件下平衡常数为K,曲线Ⅰ对应条件下平衡常数为K1,曲线Ⅱ对应条件下平衡常数为K2,则K、K1和K2的大小关系是:K2 >K > K1 |
| D.容器内气体平均摩尔质量不再改变说明该反应达到平衡状态 |
根据以下3个热化学方程式: 2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H =―Q1 kJ/mol
2H2S(g)+O2(g)="2S" (s)+2H2O(l) △H =―Q2 kJ/mol
2H2S(g)+O2(g)="2S" (s)+2H2O(g) △H =―Q3 kJ/mol
Q1、Q2、Q3三者关系正确的是
| A.Q1>Q2>Q3 | B.Q1>Q3>Q2 |
| C.Q3>Q2>Q1 | D.Q2>Q1>Q3 |
反应A(g)+B(g) C(g)+D(g)发生过程中的能量变化如图,△H 表示反应的焓变。
C(g)+D(g)发生过程中的能量变化如图,△H 表示反应的焓变。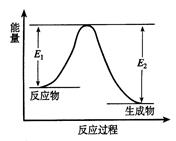
下列说法正确的是
| A.反应体系中加入催化剂,反应速率增大,E1减小,E2增大 |
| B.反应体系中加入催化剂,反应速率增大,△H不变 |
| C.△H<0,反应达到平衡时,升高温度,A的转化率增大 |
| D.△H>0,反应达到平衡时,升高温度,A的转化率减少 |
同位素示踪法可用于反应机理的研究,下列反应或转化中同位素示踪表示正确的是
| A.2Na218O2 + 2H2O = 4Nal8OH + O2↑ |
| B.2KMnO4 + 5H218O2 + 3H2SO4 = K2SO4 + 2MnSO4 + 518O2↑+ 8H2O |
C.NH4Cl + 2H2O NH3·2H2O + HCl NH3·2H2O + HCl |
| D.K37ClO3 + 6HCl = K37Cl + 3Cl2↑+ 3H2O |