短周期元素A、B、C、D的原子序数依次增大。A原子的最外层电子数是内层电子数的2倍,元素B在同周期的主族元素中原子半径最大,元素C的合金是日常生活中常用的金属材料,D位于第VIA族。下列说法正确的是( )
A.原子半径:D>B>C>A
B.元素A、B的氧化物具有相同类型的化学键
C.元素B和C的最高价氧化物对应水化物的碱性:B>C
D.B、C、D的最高价氧化物对应的水化物能相互反应
对可逆反应A(g)+B(g)="==C(g)" ΔH>0,下列图像正确的是
某温度下,体积一定的密闭容器中进行如下可逆反应: X(g)+Y(g) Z(g)+W(s);ΔH>0下列叙述正确的是
Z(g)+W(s);ΔH>0下列叙述正确的是
| A.加入少量W,逆反应速率增大 |
| B.当容器中气体压强不变时,反应达到平衡 |
| C.升高温度,平衡逆向移动 |
| D.平衡后加入X,上述反应的ΔH增大 |
下图中a曲线表示一定条件下可逆反应X(g)+Y(g)="===2Z(g)+W(S)" △H<0的反应过程。
若使a曲线变为b曲线,可采用的措施是
A 升高温度 B 增大Y的浓度 C 降低温度 D 增大体系压强
今有如下三个热化学方程式:
H2(g)+1/2O2(g)=H2O(g);ΔH=aKJ·mol-1,
H2(g)+1/2O2(g)=H2O(l);ΔH==bkJ·mol-1,
2H2(g)+O2(g)=2H2O(l);ΔH==ckJ·mol-1,
关于它们的下列表述正确的是
| A.它们都是吸热反应 | B.a、b和c均为正值 |
| C.a==b | D.2b==c |
右图是关于反应A2(g)+3B2(g)="==2C(g)" △H<0的平衡移动图形,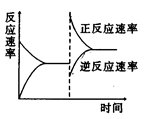
影响平衡移动的原因是
| A.升高温度,同时加压。 |
| B.降低温度,同时减压 |
| C.增大反应物浓度,同时使用催化剂; |
| D.增大反应物浓度,同时减小生成物浓度 |