空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。如图为RFC工作原理示意图。下列有关说法正确的是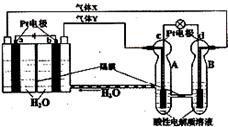
A.当有0.1 mol电子转移时,a电极产生1.12LH2
B.b电极上发生的电极反应是:4H2O +4e-=2H2↑+4OH-
C.c电极上进行还原反应,B池中的H+可以通过隔膜进入A池
D.d电极上发生的电极反应是: O 2+4H++4e-=2H2O
铜粉加入稀盐酸中,加热无现象,这时加入一种盐则铜粉溶解而溶液变蓝,同时有气体放出,这种盐是
| A.FeCl2 | B.KCl | C.Na NO3 | D.Fe2(SO4) 3 |
一定量的浓硫酸与过量的镁充分反应,生成的气体是
| A.SO2 H2 | B.SO2 | C.H2 | D.无法确定 |
在常温常压下,下列各组气体不能共存的是
| A.SO2与O2 | B.H2与Cl2 | C.H2与N2 | D.NO与O2 |
要证明CO2中混有的SO2气体,不能选用的试剂是
| A.澄清石灰水 | B.品红溶液 | C.溴水 | D.酸性KMnO4溶液 |
下列反应属于人工固氮的是
| A.分离液态空气制氮气 | B.NO和O2生成NO2 |
| C.空气在雷电作用下所产生NO | D.工业合成氨 |