下列说法正确的是( )
| A.强电解质一定可溶于水 |
| B.弱电解质是指部分溶于水的化合物 |
| C.弱电解质的导电性一定弱 |
| D.强酸、强碱不一定抑制弱酸弱碱的电离 |
在2A + B ="3C" + 4D的反应中,下列表示该反应速率最大的是
A.v(A)="0.8mol" / (L·min) B.v(B)="0.3mol" / (L·min)
C.v(C)="0.5mol" / (L·min) D.v(D)=" 1mol" / (L·min)
SF6是一种优良的绝缘气体,分子结构中只存在S-F键。已知:1molS(s)转化为气态硫原子吸收能量280 kJ,断裂1molF-F 、S-F键需吸收的能量分别为160 kJ、330 kJ。则S(s)+3F2(g)=SF6(g)的反应热△H为
| A.-1780kJ/mol | B.-1220 kJ/mol | C.-450 kJ/mol | D.+430 kJ/mol |
反应A(g)+B(g) C(g)+D(g)过程中的能量变化如图所示,
C(g)+D(g)过程中的能量变化如图所示, 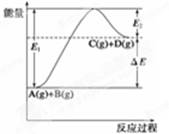
①正反应为放热反应,②反应物总能量低于生成物总能量,③反应物的总键能小于生成物的总键能,④1molA与1molB充分反应后,能量变化为ΔE,⑤加入催化剂后,反应加快,ΔE减小,⑥反应达到平衡时,升高温度,A的转化率增大,⑦升高温度可增大正反应速率,降低逆反应速率,⑧E2是反应C(g)+D(g)  A(g)+B(g)的活化能,以上有关说法正确的是
A(g)+B(g)的活化能,以上有关说法正确的是
| A.⑤⑥⑦⑧ | B.①②③④ | C.①③⑤⑦ | D.②⑥⑧ |
下列有关说法正确的是
| A.放热反应在任何条件都能自发进行 |
| B.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| C.任何能使熵值增大的过程都能自发进行 |
| D.△H>0,△S<0的化学反应一定能自发进行 |
下列反应属于放热反应的是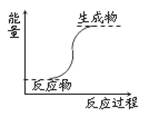
| A.能量变化如图所示的反应 |
| B.燃烧反应和铝热反应 |
| C.化学键断裂吸收的热量比化学键生成放出的热量多的反应 |
| D.氢氧化钡晶体和氯化铵晶体的反应 |