向含n mol 硫酸铝的溶液中加入m mol NaOH溶液,观察到的现象是先有白色沉淀生成,后部分溶解,则生成Al(OH)3沉淀的物质的量是
| A.(8n-m)mol | B.(4m-n)mol | C.(4n-m)mol | D.(7n-m)mol |
下列事实,能用勒夏特列原理解释的是( )
A.溴水中有平衡:Br2+ H2O  HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅 HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅 |
B.对CO(g) + NO2 (g) CO2 (g)+ NO(g) 平衡体系,增大压强可使颜色变深 CO2 (g)+ NO(g) 平衡体系,增大压强可使颜色变深 |
| C.工业上合成SO3,使用催化剂 |
| D.合成 NH3反应,在较高温度下进行 |
对于处于化学平衡状态的反应C(s) + H2O(g) 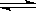 CO(g) + H2(g) △H>0,既要提高反应速率又要提高H2O的转化率,下列措施中可行的是 ( )
CO(g) + H2(g) △H>0,既要提高反应速率又要提高H2O的转化率,下列措施中可行的是 ( )
| A.增大C的量 | B.降低压强 | C.升温 | D.使用合适的催化剂 |
在一定温度下,可逆反应X(g)+3Y(g) 2Z(g)已达到平衡的是
2Z(g)已达到平衡的是
| A.单位时间内消耗n mol X同时生成2n mol Z |
| B.单位时间生成a molX同时生成3a molY |
| C.X、Y、Z的浓度不再变化 |
| D.X、Y、Z的分子数之比为1∶3∶2 |
在不同情况下测得A(g)+3B(g) 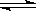 2C(g)+2D(g)的下列反应速率,其中反应速率最大的是( )
2C(g)+2D(g)的下列反应速率,其中反应速率最大的是( )
A.υ(D)="0.4" mol·L-1·s-1 B.υ(C)="0.5" mol·L-1·s-1
C.υ(B)="0.6" mol·L-1·s-1 D.υ(A)="0.15" mol·L-1·s-1
有A、B、C、D四种金属,当A、B组成原电池时,电子流动方向A →B ;当A、D组成原电池时,A为正极;B与C构成原电池时,电极反应式为:C2++2e-→C,B—2e-→B2+则A、B、C、D金属性由强到弱的顺序为()
A.A>B>C>D B.A>B>D>C C.D>A>B>C D.D>C>A>B