向含Na2CO3、NaAlO2的混合溶液中逐滴加入150 mL 1 mol·L-1 HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法不正确的是
| A.a曲线表示的离子方程式为:AlO2-+H++H2O=Al(OH)3↓ |
| B.b和c曲线表示的离子反应是相同的 |
| C.M点时,溶液中沉淀的质量为3.9 g |
| D.原混合溶液中的CO32-与AlO2-的物质的量之比为1∶2 |
下列与有机物的结构、性质有关的叙述不正确的是
| A.甲烷和乙烯都可以与氯气反应,反应类型不同 |
| B.蔗糖、油脂、蛋白质都可以水解 |
| C.乙烯和氯乙烯都可以通过聚合反应得到高分子材料 |
| D.乙醇和乙酸都存在碳氧双键,二者可以发生酯化反应 |
元素的原子结构决定其性质和在周期表中的位置,下列说法正确的是
| A.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
B.某微粒的结构示意简图为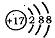 ,则该元素在周期表中位于第三周期、VIA族 ,则该元素在周期表中位于第三周期、VIA族 |
| C.Be(OH)2的碱性比Mg(OH)2的碱性强 |
| D.原子半径:Na>Si>O |
下列叙述正确的是
| A.相同条件下,等质量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多 |
| B.2 L 0.05 mol·L-1乙酸溶液中H+数为0.1NA(NA为阿伏加德罗常数) |
| C.SO2溶于水,其水溶液能导电,说明SO2是电解质 |
| D.常温下在pH=1的溶液中Na+、NH4+、[Al(OH)4]-、SO42-可以大量共存 |
化学与环境、材料、信息、能源关系密切,下列说法错误的是
| A.利用催化设施,可以将汽车尾气中CO和NO转化为无害气体 |
| B.半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 |
| C.2012年3月修订的《环境空气质量标准》中新纳入的监测指标是PM2.5 |
| D.防止酸雨发生的重要措施之一是使用清洁能源 |
人体血液里存在如下平衡:CO2+H2O H2CO3
H2CO3 HCO3-使人体血液pH值保持在7.35~7.45之间,否则就会发生酸中毒或碱中毒。其pH值随c(HCO3-):c(H2CO3)变化关系如下表所示,则下列说法中正确的是
HCO3-使人体血液pH值保持在7.35~7.45之间,否则就会发生酸中毒或碱中毒。其pH值随c(HCO3-):c(H2CO3)变化关系如下表所示,则下列说法中正确的是
| c(HCO3-):c(H2CO3) |
1.0 |
17.8 |
20.0 |
22.4 |
| pH |
6.10 |
7.35 |
7.40 |
7.45 |
A.正常人体血液中,HCO3-的水解程度小于电离程度
B.人体发生酸中毒时,可饮用碳酸饮料缓解
C.pH=7.00的血液中,c(HCO3-)=c(H2CO3)
D.常温下pH=7.40的血液稀释至pH=7.35,c(H+)·c(OH-)一定不变