中学化学中常见的几种物质存在下图所示的转化关系。其中, A是一种黑色粉末状固体,C是一种黄绿色气体,实验室中常用E溶液吸收多余的C。(图中部分产物和反应条件已略去)。
试回答下列问题:
(1)写出A与B的浓溶液反应的化学方程式 。
(2)将B的浓溶液与H的浓溶液混合,立即产生大量气体C,该反应的离子方程式为 。
(3)某课外小组同学用E溶液吸收C,利用下图所示装置向吸收液中持续通入SO2气体。实验过程中观察到如下现象:
①开始时,溶液上方出现白雾,试纸a变红。甲同学认为是HCl使a变红,乙同学不同意甲的观点,乙同学认为使a变红的是
(写出一种即可)。
②片刻后,溶液上方出现黄绿色气体,试纸b变蓝。用离子方程式解释b变蓝的原因: 。
③最终试纸b褪色。同学们认为可能的原因有两种:一是I2有还原性,黄绿色气体等物质将其氧化成IO3-,从而使蓝色消失;二是 。
下表是元素周期表的一部分:
族 |
I A |
II A |
III A |
IV A |
V A |
VI A |
VII A |
||
| 2 |
② |
③ |
④ |
⑤ |
⑥ |
||||
| 3 |
⑦ |
⑧ |
⑨ |
⑩ |
 |
 |
(1)表中元素⑩的氢化物的化学式为___________,此氢化物的还原性比元素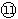 的氢化物的还原性______稳定性 (填强或弱)
的氢化物的还原性______稳定性 (填强或弱)
(2)某元素的原子结构示意图为: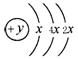 ,在周期表位于 。该
,在周期表位于 。该
氢化物沸点比甲烷 (填高或低)。
(3)用电子式表示 与⑧形成化合物形成过程: 。
与⑧形成化合物形成过程: 。
(4)写出⑦与⑨、⑨与 的最高价氧化物对应水化物反应的离子方程式:
的最高价氧化物对应水化物反应的离子方程式:
⑦与⑨: 、⑨与 。
。
如图所示,组成一种原电池.试回答下列问题(灯泡功率合适):
(1)电解质溶液为稀H2SO4时,灯泡_______(填“亮”或“不亮”,填“亮”做a题,填“不亮”做b题).
a.若灯泡亮,则Mg电极上发生的反应为: ____
Al电极上发生的反应为:____________
b.若灯泡不亮,其理由为:____________________________
(2)电解质溶液为NaOH(aq)时,灯泡__________
(填“亮”或“不亮”, 填“亮”做a题,填“不亮”做b题).
a.若灯泡亮,则Mg电极上发生的反应为:________
Al电极上发生的反应为:。
b.若灯泡不亮,其理由为:___________ ________。
(1)在下列物质中:
| A.氩 | B.NaOH | C.甲烷 | D.氯化钡(E)乙烯(F)NH3(G)CCl4(H)H2O2 ①只含离子键的物质是_____________;②既有离子键又有共价键的化合物是__________;③只含极性键的物质是__________ ;④含非极性键的物质是____________;(选填序号) |
(2)下列变化①碘的升华②烧碱熔化③氯化钠溶于水④氯化氢溶于水⑤氧气溶于水⑥氯化铵受热分解。未发生化学键破坏的是;仅发生离子键破坏的是_____;仅发生共价键破坏的是;
下表为元素周期表的一部分。请回答下列问题:
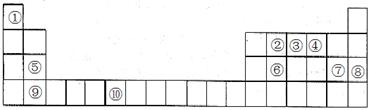
(1)上述元素中,属于s区的是________________________(填元素符号)。
(2)写出元素⑩的基态原子的电子排布式___________________________。
(3)元素第一电离能为⑤________________________⑨(填“大于”或“小于”)。
(4)元素③气态氢化物的中心原子有________________________对弧对电子,其VSEPR模型为________________________;中心原子的杂化类型为_______________;该分子为_________________分子(填“极性”或“非极性”)。向AgNO3溶液中逐滴加入其水溶液,可观察到的现象为________________________。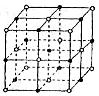
(5)元素⑦的钠盐晶胞结构如上图所示,每个Na+周围与之距离最近的Na+的个数为________________________。若设该晶胞的棱长为a cm,阿伏加德罗常数的值为NA,则该钠盐的密度为________________________(写出计算式)。
在HF、H2O、NH3、CH4、N2、CO2、HI分子中:
(1)以非极性键结合的非极性分子是。
(2)以极性键相结合,具有正四面体结构的非极性分子是。
(3)以极性键相结合,具有三角锥结构的极性分子是。
(4)以极性键相结合,具有V结构的极性分子是。
(5)以极性键相结合,而且分子极性最大的是。